Įkvėpimo formos. Farmakologinė grupė – Gliukokortikosteroidai Inhaliuojamieji gliukokortikosteroidai bronchinei astmai gydyti
Dėl citatos: Princas N.P. Gliukokortikosteroidai gydant bronchinę astmą // Krūties vėžys. 2002. Nr.5. 245 p
Rusijos valstybinio medicinos universiteto Federalinio vidaus ligų instituto Pulmonologijos skyrius
IN Pastaraisiais metais buvo pasiekta didelė pažanga gydymo srityje bronchinė astma (BA). Matyt, taip yra dėl to, kad astma apibrėžiama kaip lėtinė uždegiminė kvėpavimo takų liga ir dėl to plačiai naudojami inhaliaciniai vaistai. gliukokortikosteroidai (GCS) kaip pagrindiniai priešuždegiminiai vaistai. Tačiau nepaisant pasiektos pažangos, ligos eigos kontrolės lygis negali būti laikomas patenkinamu. Pavyzdžiui, beveik kas trečias astma sergantis pacientas bent kartą per mėnesį prabunda naktimis dėl ligos simptomų. Daugiau nei pusė pacientų turi fizinio aktyvumo apribojimus, o daugiau nei trečdalis yra priversti praleisti mokyklą arba nebūti darbe. Daugiau nei 40 % ligonių dėl ligos paūmėjimo priversti kreiptis skubios pagalbos. Šios situacijos priežastys yra įvairios, o ne mažesnį vaidmenį vaidina gydytojo nesuvokimas apie astmos patogenezę ir, atitinkamai, netinkamos gydymo taktikos pasirinkimas.
Astmos apibrėžimas ir klasifikacija Bronchinė astma yra lėtinė kvėpavimo takų liga, kurioje dalyvauja daug ląstelių: putliosios ląstelės, eozinofilai ir T-limfocitai. Jautriems asmenims šis uždegimas sukelia pasikartojančius švokštimo, dusulio, spaudimo krūtinėje ir kosulio epizodus, ypač naktį ir (arba) anksti ryte. Šiuos simptomus lydi plačiai paplitusi, bet kintama bronchų obstrukcija, kuri bent iš dalies praeina savaime arba gydant. Uždegimas taip pat sukelia kvėpavimo takų reakciją į įvairius dirgiklius (hiperreagavimą).
Reikėtų atsižvelgti į šias pagrindines apibrėžimo nuostatas:
1. Astma yra lėtinė nuolatinė uždegiminė kvėpavimo takų liga, nepriklausomai nuo sunkumo.
2. Uždegiminis procesas sukelia bronchų hiperreaktyvumą, obstrukciją ir kvėpavimo takų simptomų atsiradimą.
3. Kvėpavimo takų obstrukcija yra bent iš dalies grįžtama.
4. Atopija – genetinis polinkis gamintis E klasės imunoglobulinams (gali būti ne visada).
Bronchinė astma gali būti klasifikuojama pagal etiologiją, sunkumą ir bronchų obstrukcijos pasireiškimo požymius.
Tačiau šiuo metu bronchinę astmą pirmiausia reikėtų klasifikuoti pagal sunkumą, nes būtent tai atspindi kvėpavimo takų uždegiminio proceso sunkumą ir nulemia priešuždegiminio gydymo taktiką.
Sunkumas nustatoma pagal šiuos rodiklius:
- Naktinių simptomų skaičius per savaitę.
- Dienos simptomų skaičius per dieną ir per savaitę.
- Trumpo veikimo b 2 -agonistų vartojimo dažnis.
- Fizinio aktyvumo ir miego sutrikimų sunkumas.
- Didžiausio iškvėpimo srauto (PEF) vertės ir jo procentas su tinkama arba geriausia verte.
- Kasdieniai PSV svyravimai.
- Suteiktos terapijos apimtis.
Skiriami 5 astmos sunkumo laipsniai: lengva protarpinė; lengvas patvarus; vidutinio sunkumo nuolatinis; sunkus patvarus; sunkus nuolatinis priklausomas nuo steroidų (1 lentelė).
BA su pertrūkiais: astmos simptomai rečiau nei kartą per savaitę; trumpi paūmėjimai (nuo kelių valandų iki kelių dienų). Nakties simptomai 2 kartus per mėnesį ar rečiau; simptomų nebuvimas ir normali plaučių funkcija tarp paūmėjimų: didžiausias iškvėpimo srautas (PEF) > 80% prognozuojamas, o PEF svyravimai mažesni nei 20%.Lengva nuolatinė astma. Simptomai kartą per savaitę arba dažniau, bet rečiau nei kartą per dieną. Ligos paūmėjimai gali sutrikdyti aktyvumą ir miegą. Nakties simptomai pasireiškia dažniau nei du kartus per mėnesį. PEF yra daugiau nei 80% tikėtinos vertės; PSV svyravimai 20-30%.
Vidutinio sunkumo astma. Dienos simptomai. Paūmėjimai sutrikdo aktyvumą ir miegą. Nakties simptomai pasireiškia dažniau nei kartą per savaitę. Kasdienis trumpo veikimo b2 agonistų vartojimas. PSV 60-80% mokėtinos sumos. PEF svyravimai yra daugiau nei 30%.
Sunki astma: nuolatiniai simptomai, dažni paūmėjimai, dažni naktiniai simptomai, fizinis aktyvumas, kurį riboja astmos simptomai. PEF yra mažesnis nei 60 % numatomos vertės; svyravimai daugiau nei 30%.
Pažymėtina, kad astmos sunkumą pagal šiuos rodiklius nustatyti galima tik prieš pradedant gydymą. Jei pacientas jau gauna reikiamą gydymą, reikia atsižvelgti ir į jo kiekį. Taigi, jei paciento klinikinėje nuotraukoje nustatoma lengva persistuojanti astma, tačiau tuo pat metu jam skiriamas sunkią persistuojančią astmą atitinkantis gydymas vaistais, tai pacientui diagnozuojama sunki astma.
Sunki nuo steroidų priklausoma astma: Nepriklausomai nuo klinikinio vaizdo, pacientas, ilgai gydomas sisteminiais kortikosteroidais, turi būti laikomas sergančiu sunkia astma.
Inhaliuojami kortikosteroidai Rekomenduojamas laipsniškas požiūris į astmos gydymą priklausomai nuo jos eigos sunkumo (1 lentelė). Visi vaistai astmai gydyti skirstomi į dvi pagrindines grupes: ilgalaikei uždegiminio proceso kontrolei ir ūmių astmos simptomų palengvinimui. Ilgalaikės uždegiminio proceso kontrolės terapijos pagrindas yra inhaliaciniai gliukokortikosteroidai (ICS), kurie turėtų būti naudojami nuo antrojo etapo (lengvas persistuojantis kursas) iki penktojo (sunkus nuo steroidų priklausomas kursas). Todėl ICS šiuo metu laikomi pirmos eilės vaistais astmai gydyti. Kuo didesnė astma, tuo didesnės ICS dozės turi būti vartojamos. Daugelio tyrimų duomenimis, pacientai, kurie pradėjo gydyti IKS ne vėliau kaip per dvejus metus nuo ligos pradžios, parodė reikšmingą naudą gerinant astmos simptomų kontrolę, palyginti su grupe, kuri pradėjo gydyti IKS praėjus daugiau nei 5 metams nuo ligos pradžios. ligos.
Veikimo mechanizmai ir farmakokinetika
ICS gali prisijungti prie specifinių citoplazmos receptorių, juos aktyvuoti ir sudaryti su jais kompleksą, kuris vėliau dimerizuojasi ir persikelia į ląstelės branduolį, kur prisijungia prie DNR ir sąveikauja su pagrindinių fermentų, receptorių ir kitų kompleksų transkripcijos mechanizmais. baltymai. Tai veda prie farmakologinio ir terapinio poveikio pasireiškimo.
Priešuždegiminis ICS poveikis yra susijęs su jų slopinamu poveikiu uždegiminėms ląstelėms ir jų mediatoriams, įskaitant citokinų gamybą, trukdymą arachidono rūgšties metabolizmui ir leukotrienų bei prostaglandinų sintezei, taip pat uždegiminių ląstelių migracijos ir aktyvacijos prevencija. . ICS padidina priešuždegiminių baltymų (lipokortino-1) sintezę, padidina apoptozę ir sumažina eozinofilų skaičių, slopindami interleukiną-5. Taigi IKS stabilizuoja ląstelių membranas, mažina kraujagyslių pralaidumą, gerina b-receptorių funkciją tiek sintetindamas naujus, tiek padidindamas jų jautrumą, stimuliuoja epitelio ląsteles.
ICS skiriasi nuo sisteminių gliukokortikosteroidų savo farmakologinėmis savybėmis: lipofiliškumu, inaktyvacijos greitumu, trumpu pusinės eliminacijos iš kraujo plazmos periodu. Svarbu atsižvelgti į tai, kad gydymas ICS yra vietinis (vietinis), kuris suteikia ryškų priešuždegiminį poveikį tiesiai į bronchų medį su minimaliomis sisteminėmis apraiškomis. Į kvėpavimo takus tiekiamas ICS kiekis priklauso nuo vardinės vaisto dozės, inhaliatoriaus tipo, propelento buvimo ar nebuvimo ir įkvėpimo technikos. Iki 80 % pacientų patiria sunkumų naudojant dozuojamus aerozolius.
Svarbiausia charakteristika, leidžianti pasireikšti vaisto selektyvumui ir sulaikymo laikui audiniuose lipofiliškumas. Dėl savo lipofiliškumo ICS kaupiasi kvėpavimo takuose, lėtina jų išsiskyrimą iš audinių ir padidina afinitetą gliukokortikoidų receptoriams. Labai lipofiliniai ICS greičiau ir geriau pasisavinami iš bronchų spindžio ir ilgai išlieka kvėpavimo takų audiniuose. ICS nuo sisteminių vaistų skiriasi vietiniu (vietiniu) poveikiu. Todėl inhaliuojamųjų sisteminių kortikosteroidų (hidrokortizono, prednizolono ir deksametazono) skirti nenaudinga: šie vaistai, nepriklausomai nuo vartojimo būdo, turi tik sisteminį poveikį.
Daugybė atsitiktinių imčių, placebu kontroliuojamų tyrimų, kuriuose dalyvavo astma sergantys pacientai, parodė visų ICS dozių veiksmingumą, palyginti su placebu.
Sistema biologinis prieinamumas susideda iš geriamojo ir įkvėpimo. Nuo 20 iki 40% įkvėptos vaisto dozės patenka į kvėpavimo takus (ši vertė labai skiriasi priklausomai nuo pristatymo priemonės ir paciento įkvėpimo technikos). Plaučių biologinis prieinamumas priklauso nuo vaisto, pasiekiančio plaučius, procento, nešiklio buvimo ar nebuvimo (geriausius rezultatus pasiekia inhaliatoriai, kuriuose nėra freono) ir nuo vaisto absorbcijos kvėpavimo takuose. 60-80% įkvėptos dozės nusėda burnos ertmėje ir nuryjama, o vėliau visiškai arba iš dalies metabolizuojama virškinimo trakte ir kepenyse. Galimybė vartoti per burną priklauso nuo absorbcijos virškinimo trakte ir nuo „pirmojo praėjimo“ poveikio per kepenis, dėl kurio į sisteminę kraujotaką patenka neaktyvūs metabolitai, sunkumo (išskyrus beklometazono 17-monopropionatą, aktyvų beklometazono dipropionato metabolitą). . ICS dozės iki 1000 mikrogramų per parą (flutikazono iki 500 mikrogramų per parą) neturi sisteminio poveikio.
Visi ICS turi greitą sistemos klirensas, panašus į kepenų kraujotakos mastą. Tai vienas iš veiksnių, mažinančių sisteminį IKS poveikį.
Dažniausiai vartojamų vaistų charakteristikos
ICS yra beklometazono dipropionatas, budezonidas, flutikazono propionatas, flunizolidas, triamsinolono acetonidas, mometazono furoatas. Jie tiekiami dozuotų aerozolių, miltelių inhaliatorių, taip pat inhaliacinių tirpalų per purkštuvą (budezonido) pavidalu.
Beklometazono dipropionatas . Klinikinėje praktikoje jis naudojamas daugiau nei 20 metų ir išlieka vienu veiksmingiausių ir dažniausiai vartojamų vaistų. Leidžiama vartoti vaistą nėščioms moterims. Galima įsigyti kaip dozuotą aerozolinį inhaliatorių (Bekotide 50 mcg, Bekloforte 250 mcg, Aldecin 50 mcg, Beklocort 50 ir 250 mcg, Beclomet 50 ir 250 mcg/dozėje), kvėpuojant aktyvuojamą dozuotą dozuotą Brekotide ir Easyathing dozuojamą dozę 250 mcg/dozėje), miltelių inhaliatorius (Bekodisk 100 ir 250 mcg/dozėje, Diskhaler inhaliatorius; Easyhaler kelių dozių inhaliatorius, Beklomet 200 mcg/dozėje). Bekotide ir Bekloforte inhaliatoriams gaminami specialūs tarpikliai - „Volyumatic“ (didelio tūrio vožtuvo tarpiklis suaugusiems) ir „Babyhaler“ (mažo tūrio 2 vožtuvų tarpiklis su silikonine veido kauke mažiems vaikams).
Budezonidas . Šiuolaikinis, labai aktyvus vaistas. Naudojamas kaip dozuojamas aerozolinis inhaliatorius (Budesonide-mite 50 mcg/dozėje; Budesonide-forte 200 mcg/dozėje), miltelių inhaliatorius (Pulmicort Turbuhaler 200 mcg/dozėje; Benacort Cyclohaler 200 mcg/dozėje) ir nebuliu mg/dozėje). Pulmicort Turbuhaler yra vienintelė ICS dozavimo forma, kurioje nėra nešiklio. Dozuojamų dozių inhaliatoriams Budesonide Mite ir Budesonide Forte gaminamas tarpiklis. Budezonidas yra sudėtinio vaisto Symbicort dalis.
Budezonidas turi palankiausią terapinį indeksą, kuris yra susijęs su dideliu jo afinitetu gliukokortikoidų receptoriams ir pagreitėjusiu metabolizmu po sisteminės absorbcijos plaučiuose ir žarnyne. Budezonidas yra vienintelis ICS, kuriam buvo įrodytas vienkartinės dozės naudojimas. Budezonido veiksmingumą vieną kartą per dieną užtikrinantis veiksnys yra budezonido susilaikymas kvėpavimo takuose intraląstelinio depo pavidalu dėl grįžtamojo esterinimo (riebalų rūgščių esterių susidarymo). Sumažėjus laisvojo budezonido koncentracijai ląstelėje, suaktyvėja viduląstelinės lipazės, o iš esterių išsiskiriantis budezonidas vėl jungiasi prie receptoriaus. Šis mechanizmas nėra būdingas kitiems kortikosteroidams ir leidžia pailginti priešuždegiminį poveikį. Daugybė tyrimų parodė, kad tarpląstelinis saugojimas gali būti svarbesnis vaisto aktyvumo požiūriu nei receptorių afinitetas.
Naujausi tyrimai dėl vaisto Pulmicort Turbuhaler įrodė, kad jis neturi įtakos galutiniam vaikų augimui, kaulų mineralizacijai, nesukelia angiopatijos ir kataraktos. Pulmicort rekomenduojama vartoti ir nėščiosioms: nustatyta, kad jo vartojimas nepadidina vaisiaus anomalijų. Pulmicort Turbuhaler yra pirmoji ir vienintelė ICS, kuriai FDA (Jungtinių Valstijų vaistų kontrolės organizacija) nėštumo metu skiriamų vaistų reitinge priskyrė „B“ kategoriją. Šiai kategorijai priklauso vaistai, kuriuos saugu vartoti nėštumo metu. Likę ICS priklauso „C“ kategorijai (nėštumo metu jų vartoti nerekomenduojama).
Flutikazono propionatas . Aktyviausias vaistas iki šiol. Išgertas biologinis prieinamumas yra minimalus (<1%). Эквивалентные терапевтические дозы флютиказона почти в два раза меньше, чем у беклометазона и будесонида в аэрозольном ингаляторе и сопоставимы с дозами будесонида в Турбухалере (табл. 2). По данным ряда исследований, флютиказона пропионат больше угнетает надпочечники, но в эквивалентных дозах имеет сходную с другими ИГКС активность в отношении надпочечников.
Pateikiamas dozuojamo aerozolinio inhaliatoriaus (Flixotide 50, 125 ir 250 mcg/dozėje) ir miltelių inhaliatoriaus (Flixotide Diskhaler – rotadiskai 50, 100, 250 ir 500 mcg/dozėje; Flixotide 50, 125 ir 250 mcg/dozė; Flixotide/250 mcg/dozė) pavidalu. Aerozoliniams inhaliatoriams gaminami specialūs tarpikliai – „Volyumatic“ (didelio tūrio vožtuvo tarpiklis suaugusiems) ir „Babyhaler“ (mažo tūrio 2 vožtuvų tarpiklis su silikonine veido kauke mažiems vaikams). Flutikazonas yra sudėtinio vaisto Seretide Multidisc dalis.
Flunisolidas . Vaistas, turintis mažą gliukokortikoidų aktyvumą. Vidaus rinkoje jį atstovauja Ingacort prekės ženklas (250 mcg/dozėje dozuojamas inhaliatorius su tarpikliu). Nepaisant didelių terapinių dozių, jis praktiškai neturi sisteminio poveikio dėl to, kad jau per pirmąjį praėjimą per kepenis 95% paverčiama neaktyvia medžiaga. Šiuo metu klinikinėje praktikoje naudojamas gana retai.
Triamsinolono acetonidas . Vaistas, turintis mažą hormoninį aktyvumą. Dozuojamas inhaliatorius 100 mcg/dozėje. Azmacort prekės ženklas nėra atstovaujamas Rusijos rinkoje.
Mometazono furoatas . Vaistas, turintis didelį gliukokortikoidų aktyvumą. Rusijos rinkoje jis pateikiamas tik Nazonex nosies purškalo pavidalu.
Klinikiniai tyrimai, kuriuose lyginamas ICS veiksmingumas gerinant simptomus ir kvėpavimo funkciją, rodo, kad:
- Budezonido ir beklometazono dipropionato aerozolių inhaliatoriuose tomis pačiomis dozėmis veiksmingumas praktiškai nesiskiria.
- Flutikazono propionatas suteikia tokį patį poveikį kaip ir dvigubai didesnė beklometazono ar budezonido dozė dozuotame aerozolyje.
- Budezonidas, vartojamas per Turbuhaler, turi tokį patį poveikį kaip ir dvigubai didesnė budezonido dozė dozuotame aerozolyje.
Nepageidaujamas poveikis
Šiuolaikiniai ICS yra vaistai, turintys aukštą terapinį indeksą ir aukštą saugumo profilį net ir ilgai vartojant. Skiriamas sisteminis ir vietinis nepageidaujamas poveikis. Sisteminis nepageidaujamas poveikis gali tapti kliniškai reikšmingas tik vartojant dideles dozes. Jie priklauso nuo vaisto afiniteto receptoriui, lipofiliškumo, pasiskirstymo tūrio, pusinės eliminacijos periodo, biologinio prieinamumo ir kitų veiksnių. Sisteminio nepageidaujamo poveikio rizika visoms šiuo metu turimoms ICS koreliuoja su norimu poveikiu kvėpavimo takams. Vartojant ICS vidutinėmis terapinėmis dozėmis, sumažėja sisteminio poveikio rizika.
Pagrindinis ICS šalutinis poveikis yra susijęs su jų vartojimo būdu ir yra burnos kandidozė, užkimimas, gleivinės dirginimas ir kosulys. Norint išvengti šių reiškinių, būtina tinkama įkvėpimo technika ir individualus IKS pasirinkimas.
Kombinuoti vaistai
Nepaisant to, kad ICS yra BA terapijos pagrindas, jie ne visada leidžia visiškai kontroliuoti uždegiminį procesą bronchų medyje ir atitinkamai BA apraiškas. Atsižvelgiant į tai, pagal poreikį arba reguliariai reikėjo skirti trumpo veikimo b 2 -agonistus. Taigi, skubiai reikia naujos klasės vaistų, neturinčių trūkumų, būdingų trumpo veikimo b 2 -agonistams, ir turinčios įrodytą ilgalaikį apsauginį ir priešuždegiminį poveikį kvėpavimo takams.
Sukurti ir šiuo metu plačiai naudojami ilgai veikiantys b2 agonistai, kuriuos farmacijos rinkoje atstovauja du vaistai: formoterolio fumaratas ir salmeterolio ksinafoatas. Šiuolaikinės astmos gydymo gairės rekomenduoja papildyti ilgai veikiančius b2-agonistus, jei astmos kontrolė nepakankamai kontroliuojama taikant monoterapiją inhaliuojamaisiais kortikosteroidais (pradedant nuo antrosios stadijos). Daugybė tyrimų parodė, kad inhaliuojamųjų kortikosteroidų derinys su ilgai veikiančiu b 2 -agonistu yra veiksmingesnis nei padvigubinant inhaliuojamųjų kortikosteroidų dozę, todėl žymiai pagerėja plaučių funkcija ir geriau kontroliuojami astmos simptomai. Taip pat buvo įrodyta, kad pacientams, kuriems taikomas kombinuotas gydymas, sumažėjo paūmėjimų skaičius ir žymiai pagerėjo gyvenimo kokybė. Taigi kombinuotų vaistų, kurių sudėtyje yra inhaliuojamųjų kortikosteroidų ir ilgai veikiančio b 2 agonisto, atsiradimas atspindi požiūrio į astmos gydymą raidą.
Pagrindinis kombinuotos terapijos privalumas – padidėjęs gydymo efektyvumas, kai vartojamos mažesnės IKS dozės. Be to, sujungus du vaistus viename inhaliatoriuje, pacientui lengviau vykdyti gydytojo nurodymus ir galbūt pagerėja jų laikymasis.
Seretide Multidisc . Sudedamosios dalys yra salmeterolio ksinafoatas ir flutikazono propionatas. Užtikrina aukšto lygio astmos simptomų kontrolę. Naudojamas tik kaip pagrindinė terapija, gali būti skiriamas nuo antrojo etapo. Vaistas tiekiamas įvairiomis dozėmis: 50/100, 50/250, 50/500 mcg salmeterolio/flutikazono vienoje dozėje. Multidisc yra mažo pasipriešinimo inhaliacinis prietaisas, leidžiantis jį naudoti pacientams, kurių įkvėpimo srautas sumažėjęs.
Symbicort Turbuhaler . Sudedamosios dalys yra budezonidas ir formoterolio fumaratas. Rusijos rinkoje jis pateikiamas 160/4,5 mikrogramų 1 dozėje (vaistų dozės nurodomos kaip išėjimo dozė). Svarbi Symbicort savybė yra galimybė jį naudoti tiek pagrindinei terapijai (uždegiminiam procesui kontroliuoti), tiek greitam astmos simptomų palengvinimui. Tai visų pirma lemia formoterolio savybės (greitai veikiantis) ir budezonido gebėjimas per 24 valandas aktyviai veikti bronchų medžio gleivinę.
Symbicort leidžia individualiai lanksčiai dozuoti (1-4 inhaliacinės dozės per dieną). Symbicort galima vartoti nuo 2 stadijos, tačiau jis ypač skirtas pacientams, sergantiems nestabilia astma, kuriai būdingi staigūs sunkūs kvėpavimo priepuoliai.
Sistema GCS Sisteminiai kortikosteroidai daugiausia naudojami astmos paūmėjimui palengvinti. Geriamieji kortikosteroidai yra veiksmingiausi. Intraveniniai kortikosteroidai skiriami astmos paūmėjimui, jei labiau pageidautina patekti į veną arba esant sutrikusiam rezorbcijai iš virškinimo trakto, vartojant dideles dozes (iki 1 g prednizolono, metilprednizolono ir hidrokortizono). Kortikosteroidai kliniškai reikšmingai pagerėjo praėjus 4 valandoms po jų vartojimo.
BA paūmėjimo metu nurodomas trumpas geriamųjų kortikosteroidų kursas (7-14 dienų), pradedant nuo didelių dozių (30-60 mg prednizolono). Naujausiose publikacijose rekomenduojamas toks trumpas sisteminių kortikosteroidų kursas esant gyvybei nepavojingiems paūmėjimams: 6 prednizolono tabletės ryte (30 mg) 10 dienų, po to vartojimą nutraukti. Nors gydymo sisteminiais kortikosteroidais schemos gali būti skirtingos, pagrindiniai principai yra jų skyrimas didelėmis dozėmis, kad būtų greitai pasiektas poveikis, o vėliau greitai nutraukiama. Reikia atsiminti, kad kai tik pacientas yra pasiruošęs vartoti inhaliuojamųjų kortikosteroidų, jie jam turi būti skiriami laipsniškai.
Sisteminiai gliukokortikoidai turi būti skiriami, jei:
- Vidutinis ar sunkus paūmėjimas.
- Gydymo pradžioje skiriant trumpo veikimo inhaliuojamųjų b 2 -agonistų pagerėjimo nepagerėjo.
- Paūmėjimas išsivystė nepaisant to, kad pacientas buvo ilgai gydomas geriamaisiais kortikosteroidais.
- Geriamieji kortikosteroidai buvo reikalingi ankstesniems paūmėjimams kontroliuoti.
- Gliukokortikoidų kursai buvo skiriami 3 ir daugiau kartų per metus.
- Pacientui taikoma mechaninė ventiliacija.
- Anksčiau buvo gyvybei pavojingų paūmėjimų.
Nepageidautina naudoti ilgai veikiančių sisteminių steroidų formų paūmėjimui palengvinti ir astmos palaikomajam gydymui.
Ilgalaikiam sunkios astmos gydymui reikia skirti mažiausią veiksmingą sisteminio poveikio kortikosteroidų (metilprednizolono, prednizolono, triamsinolono, betametazono) dozę. Ilgai gydant, kaitaliojamas recepto režimas ir vartojimas pirmoje dienos pusėje (siekiant sumažinti poveikį cirkadiniam kortizolio sekrecijos ritmui) sukelia mažiausiai šalutinių poveikių. Pabrėžtina, kad visais sisteminio poveikio steroidų skyrimo atvejais pacientui turi būti skiriamos didelės inhaliuojamųjų kortikosteroidų dozės. Iš geriamųjų kortikosteroidų pirmenybė teikiama tiems, kurie pasižymi minimaliu mineralokortikoidų aktyvumu, santykinai trumpu pusinės eliminacijos periodu ir ribotu poveikiu ruožuotiems raumenims (prednizolonas, metilprednizolonas).
Priklausomybė nuo steroidų
Ypatingas dėmesys turėtų būti skiriamas pacientams, kurie yra priversti nuolat vartoti sisteminius kortikosteroidus. Yra keletas būdų, kaip formuoti priklausomybę nuo steroidų pacientams, sergantiems astma ir kitomis ligomis, kurias lydi bronchų obstrukcija:
- Gydytojo ir paciento nesilaikymas (sąveika).
- Neskiria pacientams inhaliuojamųjų kortikosteroidų. Daugelis gydytojų mano, kad pacientams, vartojantiems sisteminius steroidus, nereikia skirti inhaliuojamųjų kortikosteroidų. Jei astma sergantis pacientas vartoja sisteminius steroidus, jis turi būti laikomas sunkia astma sergančiu pacientu, kuriam yra tiesioginė indikacija vartoti dideles inhaliuojamųjų kortikosteroidų dozes.
- Pacientams, sergantiems sisteminėmis ligomis (įskaitant plaučių vaskulitą, pavyzdžiui, Charge-Strauss sindromą), bronchų obstrukcija gali būti laikoma astma. Sisteminių steroidų vartojimo nutraukimas šiems pacientams gali lydėti sunkių sisteminės ligos apraiškų.
- 5% atvejų atsiranda atsparumas steroidams, kuriam būdingas steroidų receptorių atsparumas steroidiniams vaistams. Šiuo metu išskiriami du pogrupiai: pacientai, kuriems nustatytas tikrasis atsparumas steroidams (II tipas), kuriems ilgą laiką vartojant dideles sisteminių kortikosteroidų dozes nepasireiškia šalutinis poveikis, ir pacientai, kurių atsparumas įgytas (I tipas), kuriems pasireiškia šalutinis poveikis: sisteminiai kortikosteroidai. Pastarajame pogrupyje atsparumą greičiausiai galima įveikti didinant GCS dozę ir skiriant adityvaus poveikio vaistus.
1. Bronchinė astma. Pasaulinė strategija: bendra Nacionalinio širdies, plaučių ir kraujo instituto bei Pasaulio sveikatos organizacijos ataskaita. Pulmonologija, 1996 m.
2. Bronchinė astma. Vadovas gydytojams Rusijoje (formulinė sistema). “Pulmonologija”, priedas-99.
3. Pagrindinės bronchinės astmos diagnostikos ir gydymo kryptys. Svarbiausi EPR-2 ekspertų grupės ataskaitos akcentai. Nacionalinis sveikatos institutas. Nacionalinis širdies, plaučių ir kraujo institutas. NIH leidinys-97. Vertimas red. Prof. Tsoi A.N., M, Grantas, 1998 m.
4. Iljina N.I. Inhaliuojami gliukokortikoidai. Asthma.ru. Alerginės ir kvėpavimo takų ligos. 0*2001 (pilotinis epizodas).
5. Ogorodova L.M. Sistemos, skirtos vaistų tiekimui į kvėpavimo takus įkvėpus. Pulmonologija, 1999; Nr.1, 84-87
6. Formulės sistema: bronchinės astmos gydymas. Astma. ru ,0. 2001, 6-9
7. Chuchalin A.G. Bronchų astma. Maskva, 1997 m.
8. Tsoi A.N. Inhaliuojami gliukokortikoidai: veiksmingumas ir saugumas. RMJ 2001; 9: 182-185
9. Tsoi A.N. Inhaliuojamųjų gliukokortikoidų lyginamoji farmakokinetika. Alergologija 1999; 3:25-33
10. Agertoft L., Pedersen S. Ilgalaikio gydymo inhaliuojamuoju budezonidu poveikis suaugusiųjų ūgiui astma sergantiems vaikams. N Engl J Med 2000; 343:1064-9
11. Ankerst J., Persson G., Weibull E. Didelę budezonido/formoterolio dozę viename inhaliatoriuje gerai toleravo astma sergantys pacientai. Eur Respir J 2000; 16 (31 priedas): 33s + plakatas
12. Barnesas P.J. Inhaliaciniai gliukokortikoidai astmai gydyti. N.Angl. Med. 1995 m.; 332:868-75
13. Beklometazono dipropionatas ir budezonidas. Klinikiniai įrodymai peržiūrėti. Respir Med 1998; 92 (priedas B)
14. Britanijos astmos valdymo gairės. Krūtinė, 1997; 52 (1 priedas) 1-20.
15. Burney PGJ. Aktualūs astmos epidemiologijos klausimai Holgate ST ir kt., Astma: Physiology. Imunologija ir gydymas. Londonas, Academic Press, 1993, p. 3-25.
16. Crisholm S ir kt. Vieną kartą per parą vartojamas budezonidas sergant lengva astma. Respir Med 1998; 421-5
17. Kips JC, O/Connor BJ, Inman MD, Svensson K, Pauwels RA, O/Byrne PM. Ilgalaikis mažos budezonido ir formoterolio dozės priešuždegiminio poveikio, palyginti su didelėmis budezonido dozėmis astma, tyrimas. Am Respir Crit Care Med 2000; 161:996-1001
18. McFadden ER, Casale TB, Edwards TB ir kt. Budezonido vartojimas vieną kartą per parą naudojant Turbuhaler pacientams, sergantiems stabilia astma. J Allergy Clin Immunol 1999; 104:46-52
19. Miller-Larsson A., Mattsson H., Hjertberg E., Dahlback M., Tunek A., Brattsand R. Grįžtamoji budezonido riebalų rūgščių konjugacija: naujas mechanizmas ilgalaikiam lokaliai vartojamo steroido susilaikymui kvėpavimo takų audinyje. Drug Metab Dispos 1998; 26: 623-30
20. Miller-Larsson A. ir kt. Pailgėjęs kvėpavimo takų aktyvumas ir pagerėjęs budezonido selektyvumas galbūt dėl esterifikacijos. Am J Respir Crit Care Med 2000;162:1455-1461
21. Pauwels RA ir kt. Inhaliuojamo formoterolio ir budezonido poveikis astmos paūmėjimui. N Engl J Med 1997; 337:1405-11
22. Pedersen S, O/Byrne P. Inhaliuojamųjų kortikosteroidų veiksmingumo ir saugumo palyginimas sergant astma. Alergija 1997; 52 (39 priedas): 1–34.
23. Woolcock A. ir kt. Salmeterolio pridėjimo prie inhaliuojamųjų steroidų palyginimas su inhaliuojamųjų steroidų dozės padvigubėjimu. Am J Respir Crit Care Med 1996, 153, 1481-8.
Ačiū
Svetainėje pateikiama informacinė informacija tik informaciniais tikslais. Ligų diagnostika ir gydymas turi būti atliekami prižiūrint specialistui. Visi vaistai turi kontraindikacijų. Būtina konsultacija su specialistu!
Įvadas (vaistų savybės)
Natūralūs kortikosteroidai
 Kortikosteroidai- Dažnas vardas hormonai antinksčių žievė, kurią sudaro gliukokortikoidai ir mineralokortikoidai. Pagrindiniai žmogaus antinksčių žievėje gaminami gliukokortikoidai yra kortizonas ir hidrokortizonas, o mineralokortikoidas – aldosteronas.
Kortikosteroidai- Dažnas vardas hormonai antinksčių žievė, kurią sudaro gliukokortikoidai ir mineralokortikoidai. Pagrindiniai žmogaus antinksčių žievėje gaminami gliukokortikoidai yra kortizonas ir hidrokortizonas, o mineralokortikoidas – aldosteronas. Kortikosteroidai atlieka daug labai svarbių funkcijų organizme.
Gliukokortikoidai atsižvelgti į steroidai, kurios pasižymi priešuždegiminiu poveikiu, dalyvauja reguliuojant angliavandenių, riebalų ir baltymų apykaitą, kontroliuoja brendimą, inkstų veiklą, organizmo reakciją į stresą, prisideda prie normalios nėštumo eigos. Kortikosteroidai inaktyvuojami kepenyse ir išsiskiria su šlapimu.
Aldosteronas reguliuoja natrio ir kalio metabolizmą. Taigi, esant įtakai mineralokortikoidai Na+ sulaikomas organizme ir padidėja K+ jonų išsiskyrimas iš organizmo.
Sintetiniai kortikosteroidai
Sintetiniai kortikosteroidai, pasižymintys tokiomis pat savybėmis kaip ir natūralūs, buvo praktiškai pritaikyti medicinos praktikoje. Jie gali laikinai slopinti uždegiminį procesą, tačiau neturi įtakos infekcinei ligos kilmei ar patogenams. Pasibaigus kortikosteroidų vartojimui, infekcija atsinaujina.Kortikosteroidai sukelia įtampą ir stresą organizme, o tai lemia imuniteto sumažėjimą, nes imunitetas yra pakankamas tik atsipalaidavus. Atsižvelgdami į tai, kas išdėstyta pirmiau, galime teigti, kad kortikosteroidų vartojimas prisideda prie užsitęsusios ligos eigos ir blokuoja regeneracijos procesą.
Be to, sintetiniai kortikosteroidai slopina natūralių kortikosteroidų hormonų funkciją, todėl apskritai sutrinka antinksčių veikla. Kortikosteroidai veikia kitų endokrininių liaukų veiklą ir sutrikdo hormonų pusiausvyrą organizme.
Kortikosteroidiniai vaistai, pašalinantys uždegimą, taip pat turi analgetinį poveikį. Sintetiniai kortikosteroidiniai vaistai yra deksametazonas, prednizolonas, sinalaras, triamcinolonas ir kt. Šie vaistai yra aktyvesni ir sukelia mažiau šalutinių poveikių nei natūralūs.
Kortikosteroidų išsiskyrimo formos
Kortikosteroidai gaminami tablečių, kapsulių, tirpalų ampulėse, tepalų, linimentų ir kremų pavidalu. (Prednizolonas, Deksametazonas, Budenofalmas, Kortizonas, Kortinefas, Medrolas).Vidaus vartojimo preparatai (tabletėse ir kapsulėse)
- Prednizolonas;
- Celestonas;
- triamcinolonas;
- Kenakortas;
- Cortineffas;
- Polkortolonas;
- Kenalogas;
- Metipred;
- Berlicourt;
- Florinefas;
- Medrol;
- citrinas;
- Dekadronas;
- Urbazon ir kt.
Preparatai injekcijoms
- Prednizolonas;
- Hidrokortizonas;
- Diprospanas (betametazonas);
- Kenalogas;
- Flosteronas;
- Medrol ir kt.
Preparatai vietiniam vartojimui (vietiniam)
- Prednizolonas (tepalas);
- Hidrokortizonas (tepalas);
- Lokoid (tepalas);
- Cortade (tepalas);
- Afloderm (grietinėlė);
- Laticort (grietinėlė);
- Dermovate (kremas);
- Fluorokortas (tepalas);
- Lorinden (tepalas, losjonas);
- Sinaflan (tepalas);
- Flucinar (tepalas, gelis);
- Klobetasolis (tepalas) ir kt.
Silpnai aktyvūs agentai: Prednizolonas, Hidrokortizonas, Cortade, Lokoidas;
Vidutiniškai aktyvus: Afloderm, Laticort, Dermovate, Fluorocort, Lorinden;
Labai aktyvus: Akriderm, Advantan, Kuterid, Apulein, Cutivate, Sinaflan, Sinalar, Sinoderm, Flucinar.
Labai aktyvus: Klobetasolis.
Kortikosteroidai, skirti įkvėpti

- Beklametazonas dozuotų aerozolių pavidalu (Becotide, Aldecim, Beclometas, Beclocort); bekodiskių pavidalu (vienos dozės milteliai, įkvėpti naudojant diskhalerį); dozuoto aerozolio, skirto įkvėpti per nosį, pavidalu (beclometazonas-nosinis, Beconase, Aldecim);
- Flunisolidas dozuotų aerozolių pavidalu su tarpikliu (Ingacort), skirtas vartoti į nosį (Sintaris);
- Budezonidas – dozuojamas aerozolis (Pulmicort), vartojimui į nosį – Rhinocort;
- Flutikazonas Flixotide ir Flixonase aerozolių pavidalu;
- Triamcinolonas – dozuojamas aerozolis su tarpikliu (Azmacort), vartojimui į nosį – Nazacort.
Naudojimo indikacijos
Kortikosteroidai naudojami uždegimui slopinti daugelyje medicinos šakų ir daugeliui ligų.Gliukokortikoidų vartojimo indikacijos
- Reumatas;
- reumatoidinis ir kitų tipų artritas;
- kolagenozės, autoimuninės ligos (sklerodermija, sisteminė raudonoji vilkligė, mazginis periarteritas, dermatomiozitas);
- kraujo ligos (mieloblastinė ir limfoblastinė leukemija);
- kai kurie piktybinių navikų tipai;
- odos ligos (neurodermitas, psoriazė, egzema, seborėjinis dermatitas, diskoidinė raudonoji vilkligė, atopinis dermatitas, eritrodermija, plokščioji kerpligė);
- bronchų astma;
- alerginės ligos;
- pneumonija ir bronchitas, fibrozinis alveolitas;
- opinis kolitas ir Krono liga;
- ūminis pankreatitas;
- hemolizinė anemija;
- virusinės ligos (infekcinė mononukleozė, virusinis hepatitas ir kt.);
- išorinis otitas (ūminis ir lėtinis);
- šoko gydymas ir profilaktika;
- oftalmologijoje (dėl neinfekcinių ligų: irito, keratito, iridociklito, sklerito, uveito);
- neurologinės ligos (išsėtinė sklerozė, ūminis nugaros smegenų pažeidimas, regos nervo neuritas);
- organų transplantacijos metu (siekiant nuslopinti atmetimą).
Mineralkortikoidų vartojimo indikacijos
- Adisono liga (lėtinis antinksčių hormonų trūkumas);
- myasthenia gravis (autoimuninė liga, pasireiškianti raumenų silpnumu);
- mineralų apykaitos sutrikimai;
- adinamija ir raumenų silpnumas.
Kontraindikacijos
 Kontraindikacijos gliukokortikoidų vartojimui:
Kontraindikacijos gliukokortikoidų vartojimui:- padidėjęs jautrumas vaistui;
- sunkios infekcijos (išskyrus tuberkuliozinį meningitą ir septinį šoką);
- imunizacija gyva vakcina.
Kontraindikacijos mineralokortikoidams vartoti:
- aukštas kraujo spaudimas;
- diabetas;
- mažas kalio kiekis kraujyje;
- inkstų ir kepenų nepakankamumas.
Nepageidaujamos reakcijos ir atsargumo priemonės
Kortikosteroidai gali sukelti daug įvairių šalutinių poveikių. Vartojant silpnai ar vidutiniškai aktyvius vaistus, nepageidaujamos reakcijos būna ne tokios ryškios ir pasireiškia retai. Didelės vaistų dozės ir labai aktyvių kortikosteroidų vartojimas, ilgalaikis jų vartojimas gali sukelti tokį šalutinį poveikį:- edemos atsiradimas dėl natrio ir vandens susilaikymo organizme;
- padidėjęs kraujospūdis;
- padidėjęs cukraus kiekis kraujyje (netgi galimas steroidinio diabeto išsivystymas);
- osteoporozė dėl padidėjusios kalcio sekrecijos;
- aseptinė kaulinio audinio nekrozė;
- skrandžio opos paūmėjimas ar atsiradimas; kraujavimas iš virškinimo trakto;
- padidėjęs trombų susidarymas;
- svorio priaugimas;
- bakterinių ir grybelinių infekcijų atsiradimas dėl sumažėjusio imuniteto (antrinis imunodeficitas);
- menstruacijų sutrikimai;
- neurologiniai sutrikimai;
- glaukomos ir kataraktos vystymasis;
- odos atrofija;
- padidėjęs prakaitavimas;
- spuogų atsiradimas;
- audinių regeneracijos proceso slopinimas (lėtas žaizdų gijimas);
- per didelis veido plaukų augimas;
- antinksčių funkcijos slopinimas;
- nuotaikos nestabilumas, depresija.
- riebalų perteklius tam tikrose kūno vietose: ant veido (vadinamasis „mėnulio veidas“), ant kaklo („jaučio kaklas“), krūtinėje ir pilve;
- atrofuojasi galūnių raumenys;
- mėlynės ant odos ir strijos (strijos) ant pilvo.
Norint sumažinti nepageidaujamų reakcijų riziką, svarbu operatyviai reaguoti į jų atsiradimą, koreguoti dozes (vartoti mažas dozes, kai tik įmanoma), kontroliuoti kūno svorį ir suvartojamo maisto kaloringumą, riboti valgomosios druskos ir skysčių vartojimą.
Kaip vartoti kortikosteroidus?
 Gliukokortikosteroidai gali būti naudojami sistemiškai (tablečių ir injekcijų pavidalu), lokaliai (į sąnarį, į tiesiąją žarną), lokaliai (tepalai, lašai, aerozoliai, kremai).
Gliukokortikosteroidai gali būti naudojami sistemiškai (tablečių ir injekcijų pavidalu), lokaliai (į sąnarį, į tiesiąją žarną), lokaliai (tepalai, lašai, aerozoliai, kremai). Dozavimo režimą nustato gydytojas. Vaistą tabletėmis reikia gerti nuo 6 val. ryto (pirmoji dozė), o vėlesnius – ne vėliau kaip 14 val. Tokios vartojimo sąlygos yra būtinos norint priartėti prie fiziologinio gliukokortikoidų patekimo į kraują, kai juos gamina antinksčių žievė.
Kai kuriais atvejais, vartojant dideles dozes ir priklausomai nuo ligos pobūdžio, dozę gydytojas paskirsto tolygiai per dieną į 3-4 dozes.
Tabletes reikia gerti valgio metu arba iškart po valgio, užsigeriant nedideliu kiekiu vandens.
Gydymas kortikosteroidais
Yra šie kortikosteroidų gydymo tipai:- intensyvus;
- ribojantis;
- kintamasis;
- su pertrūkiais;
- pulso terapija.
Apribojanti terapiją naudojamas ilgalaikiams, lėtiniams procesams – kaip taisyklė, tablečių formos vartojamos kelis mėnesius ar net metus.
Siekiant sumažinti slopinamąjį poveikį endokrininių liaukų funkcijai, naudojami periodiniai vaistų dozavimo režimai:
- kintamoji terapija – vartoti trumpo ir vidutinio veikimo gliukokortikoidus (prednizoloną, metilprednizoloną) vieną kartą nuo 6 iki 8 val. kas 48 valandas;
- pertraukiamas gydymas – trumpi, 3-4 dienų vaisto vartojimo kursai su 4 dienų pertraukomis tarp jų;
- pulso terapija– greitas didelės (mažiausiai 1 g) vaisto dozės į veną suleidimas skubios pagalbos atveju. Pasirinktas vaistas tokiam gydymui yra metilprednizolonas (jis labiau prieinamas paveiktoms vietovėms ir turi mažiau šalutinių poveikių).
- Mažas - mažiau nei 7,5 mg;
- Vidutinė – 7,5 -30 mg;
- Didelis – 30-100 mg;
- Labai didelis - virš 100 mg;
- Pulso terapija – virš 250 mg.
Prevencijai Jei yra nepageidaujamas kortikosteroidų poveikis virškinamajam traktui, prieš vartojant tabletes, galite rekomenduoti vartoti Almagel, želė. Rekomenduojama atsisakyti rūkymo ir piktnaudžiavimo alkoholiu; vidutinio sunkumo mankšta.
Kortikosteroidai vaikams
Sisteminiai gliukokortikoidai Vaikams skiriami tik pagal absoliučias indikacijas. Sergant bronchų obstrukcijos sindromu, kuris kelia grėsmę vaiko gyvybei, į veną skiriama 2-4 mg prednizolono 1 kg vaiko kūno svorio (priklausomai nuo ligos sunkumo), o jei poveikio nėra, dozė didinama 20-50% kas 2-4 valandas, kol pasireikš efektas. Po to vaisto vartojimas nedelsiant nutraukiamas, palaipsniui nemažinant dozės.Vaikai, turintys priklausomybę nuo hormonų (pavyzdžiui, sergantys bronchine astma), suleidę vaisto į veną, palaipsniui pereina prie palaikomosios prednizolono dozės. Esant dažniems astmos atkryčiams, beklametazono dipropionatas vartojamas inhaliacijų forma - dozė parenkama individualiai. Pasiekus poveikį, dozė palaipsniui mažinama iki palaikomosios dozės (parenkama individualiai).
Vietiniai gliukokortikoidai(kremai, tepalai, losjonai) naudojami pediatrinėje praktikoje, tačiau vaikai turi didesnį polinkį į sisteminį vaistų poveikį nei suaugusieji (uždelstas vystymasis ir augimas, Itsenko-Kušingo sindromas, endokrininių liaukų funkcijos slopinimas). Taip yra todėl, kad vaikų kūno paviršiaus ploto ir kūno masės santykis yra didesnis nei suaugusiųjų.
Dėl šios priežasties vietiniai gliukokortikoidai vaikams turėtų būti vartojami tik ribotose vietose ir trumpą kursą. Tai ypač pasakytina apie naujagimius. Vaikams pirmaisiais gyvenimo metais galite naudoti tik tepalus, kuriuose yra ne daugiau kaip 1% hidrokortizono arba ketvirtos kartos vaisto - Prednicarbate (Dermatol), o vaikams iki 5 metų - hidrokortizono 17-butiratą arba tepalus su vid. stiprumo vaistai.
Vyresniems nei 2 metų vaikams gydyti mometazoną galima vartoti taip, kaip nurodė gydytojas (tepalas, turi ilgalaikį poveikį, tepamas vieną kartą per dieną).
Vaikų atopiniam dermatitui gydyti yra ir kitų vaistų, kurių sisteminis poveikis yra ne toks ryškus, pavyzdžiui, Advantan. Galima vartoti iki 4 savaičių, tačiau jo naudojimas yra ribotas dėl vietinių nepageidaujamų reakcijų (odos išsausėjimo ir plonėjimo) galimybės. Bet kokiu atveju vaistą, skirtą vaikui gydyti, pasirenka gydytojas.
Kortikosteroidai nėštumo ir žindymo laikotarpiu
 Net ir trumpalaikis gliukokortikoidų vartojimas gali „užprogramuoti“ daugelio negimusio vaiko organų ir sistemų darbą (kraujospūdžio kontrolę, medžiagų apykaitos procesus, elgesio formavimąsi) ateinantiems dešimtmečiams. Sintetinis hormonas imituoja motinos siunčiamą streso signalą vaisiui ir taip skatina vaisius greičiau panaudoti atsargas.
Net ir trumpalaikis gliukokortikoidų vartojimas gali „užprogramuoti“ daugelio negimusio vaiko organų ir sistemų darbą (kraujospūdžio kontrolę, medžiagų apykaitos procesus, elgesio formavimąsi) ateinantiems dešimtmečiams. Sintetinis hormonas imituoja motinos siunčiamą streso signalą vaisiui ir taip skatina vaisius greičiau panaudoti atsargas. Šį neigiamą gliukokortikoidų poveikį sustiprina tai, kad šiuolaikiniai ilgai veikiantys vaistai (Metypred, Dexamethasone) nėra deaktyvuojami placentos fermentų ir turi ilgalaikį poveikį vaisiui. Gliukokortikoidai, slopindami imuninę sistemą, padeda sumažinti nėščiosios atsparumą bakterinėms ir virusinėms infekcijoms, kurios taip pat gali neigiamai paveikti vaisius.
Gliukokortikoidiniai vaistai nėščiai moteriai gali būti skiriami tik tuo atveju, jei jų vartojimo rezultatas gerokai viršija galimų neigiamų pasekmių vaisiui riziką.
Tokios indikacijos gali būti:
1.
Priešlaikinio gimdymo grėsmė (trumpas hormonų kursas pagerina priešlaikinio vaisiaus pasirengimą gimdyti); paviršinio aktyvumo medžiagos naudojimas vaikui po gimimo leido sumažinti hormonų naudojimą pagal šią indikaciją.
2.
Reumatas ir autoimuninės ligos aktyvioje fazėje.
3.
Paveldima (intrauterinė) vaisiaus antinksčių žievės hiperplazija yra sunkiai diagnozuojama liga.
Anksčiau buvo praktika skiriant gliukokortikoidus, kad palaikytų nėštumą. Tačiau įtikinamų duomenų apie šios technikos veiksmingumą negauta, todėl šiuo metu ji nenaudojama.
Akušerijos praktikoje Dažniau naudojami Metypred, Prednizolonas ir Deksametazonas. Į placentą jie prasiskverbia įvairiai: prednizoloną placentoje esantys fermentai sunaikina labiau, o deksametazoną ir metipredą – tik 50%. Todėl, jei nėščiajai gydyti vartojami hormoniniai vaistai, geriau skirti Prednizoloną, o vaisiui gydyti – Deksametazoną arba Metypredą. Šiuo atžvilgiu prednizolonas rečiau sukelia nepageidaujamas reakcijas vaisiui.
Esant stipriai alergijai, gliukokortikoidai skiriami tiek sistemiškai (injekcijos ar tabletės), tiek vietiniai (tepalai, geliai, lašai, inhaliacijos). Jie turi stiprų antialerginį poveikį. Dažniausiai naudojami šie vaistai: hidrokortizonas, prednizolonas, deksametazonas, betametazonas, beklometazonas.
Iš vietinio poveikio gliukokortikoidų (vietiniam gydymui) dažniausiai naudojami intranazaliniai aerozoliai: nuo šienligės, alerginio rinito, nosies užgulimo (čiaudėjimo). Paprastai jie turi gerą poveikį. Flutikazonas, dipropionatas, propionatas ir kiti buvo plačiai naudojami.
Sergant alerginiu konjunktyvitu, dėl didesnės šalutinio poveikio rizikos gliukokortikoidai vartojami retai. Bet kokiu atveju, esant alerginėms apraiškoms, hormoniniai vaistai negali būti naudojami savarankiškai, kad būtų išvengta nepageidaujamų pasekmių.
Kortikosteroidai psoriazei gydyti
 Gliukokortikoidai nuo psoriazės turėtų būti naudojami daugiausia tepalų ir kremų pavidalu. Sisteminiai (injekcijos ar tabletės) hormoniniai vaistai gali prisidėti prie sunkesnės psoriazės formos (pustulinės ar pustulinės) išsivystymo, todėl jų vartoti nerekomenduojama.
Gliukokortikoidai nuo psoriazės turėtų būti naudojami daugiausia tepalų ir kremų pavidalu. Sisteminiai (injekcijos ar tabletės) hormoniniai vaistai gali prisidėti prie sunkesnės psoriazės formos (pustulinės ar pustulinės) išsivystymo, todėl jų vartoti nerekomenduojama. Vietiniam vartojimui skirti gliukokortikoidai (tepalai, kremai) dažniausiai vartojami 2 kartus per dieną. per dieną: kremai dieną be tvarsčių, o naktį kartu su akmens anglių derva arba antralinu, naudojant okliuzinį tvarstį. Esant dideliems pažeidimams, viso kūno gydymui sunaudojama maždaug 30 g vaisto.
Gliukokortikoidinio vaisto pasirinkimas pagal aktyvumo laipsnį vietiniam vartojimui priklauso nuo psoriazės sunkumo ir jos paplitimo. Kadangi gydymo metu psoriazės pažeidimų mažėja, vaistą reikia keisti į mažiau aktyvų (arba vartoti rečiau), kad būtų sumažintas šalutinis poveikis. Kai poveikis pasiekiamas maždaug po 3 savaičių, hormoninį vaistą 1-2 savaites geriau pakeisti minkštikliu.
Gliukokortikoidų vartojimas dideliuose plotuose ilgą laiką gali apsunkinti procesą. Psoriazės atkrytis nutraukus vaisto vartojimą pasireiškia anksčiau nei gydant nenaudojant gliukokortikoidų.
, Coaxil, Imipramine ir kt.) kartu su gliukokortikoidais gali padidinti akispūdį.
Kortikosteroidų vartojimo nutraukimo taisyklės
Ilgai vartojant gliukokortikoidus, vaisto vartojimą reikia nutraukti laipsniškai. Gliukokortikoidai slopina antinksčių žievės funkciją, todėl greitai ar staiga nutraukus vaisto vartojimą, gali išsivystyti antinksčių nepakankamumas. Nėra standartizuoto kortikosteroidų vartojimo nutraukimo schemos. Nutraukimo ir dozės mažinimo būdas priklauso nuo ankstesnio gydymo kurso trukmės.Jei gliukokortikoidų kursas trunka iki kelių mėnesių, Prednizolono dozę galite mažinti 2,5 mg (0,5 tabletės) kas 3-5 dienas. Kurso trukmė ilgesnė, dozė mažinama lėčiau – po 2,5 mg kas 1-3 savaites. Labai atsargiai mažinkite dozę iki 10 mg – 0,25 tabletės kas 3-5-7 dienas.
Jei pradinė prednizolono dozė buvo didelė, iš pradžių ji mažinama intensyviau: po 5-10 mg kas 3 dienas. Pasiekus paros dozę, lygią 1/3 pradinės dozės, mažinti 1,25 mg (1/4 tabletės) kas 2-3 savaites. Dėl šio sumažinimo pacientas gauna palaikomąsias dozes metus ar ilgiau.
Vaistų mažinimo režimą skiria gydytojas, o šio režimo pažeidimas gali sukelti ligos paūmėjimą – gydymą teks vėl pradėti didesne doze.
Kortikosteroidų kainos
 Kadangi yra tiek daug įvairių formų kortikosteroidų, čia pateikiamos tik kelių kainos:
Kadangi yra tiek daug įvairių formų kortikosteroidų, čia pateikiamos tik kelių kainos: - Hidrokortizonas – suspensija – 1 butelis 88 rubliai; akių tepalas 3 g – 108 rubliai;
- Prednizolonas - 100 tablečių po 5 mg - 96 rubliai;
- Metypred - 30 tablečių po 4 mg - 194 rubliai;
- Metypred – 250 mg 1 buteliukas – 397 rubliai;
- Triderm - tepalas 15 g - 613 rubliai;
- Triderm – kremas 15 g – 520 rublių;
- Deksamedas – 100 ampulių po 2 ml (8 mg) – 1377 rubliai;
- Deksametazonas - 50 tablečių po 0,5 mg - 29 rubliai;
- Deksametazonas - 10 ampulių po 1 ml (4 mg) - 63 rubliai;
- Oftan Dexamethasone - akių lašai 5 ml - 107 rubliai;
- Medrol – 50 tablečių po 16 mg – 1083 rubliai;
- Fliksotidas – aerozolis 60 dozių – 603 rubliai;
- Pulmicort – aerozolis 100 dozių – 942 rubliai;
- Benacort – aerozolis 200 dozių – 393 rubliai;
- Symbicort - aerozolis su 60 dozių dozatoriumi - 1313 rublių;
- Beclazon - aerozolis 200 dozių - 475 rubliai.
Gliukokortikosteroidai kaip pagrindiniai vaistai astmai gydyti. ICS.
Kaip žinoma, bronchinės astmos eigos pagrindas yraMes (BA) sergame lėtiniu uždegimu, o pagrindinis šios ligos gydymo metodas yrapriešuždegiminių vaistų vartojimas. Šiandien gliukokortikosteroidai yra pripažintipagrindiniai vaistai astmai gydyti.
Sisteminiai kortikosteroidai ir šiandien tebėra pasirenkami vaistai gydant astmos paūmėjimą, tačiau praėjusio amžiaus 60-ųjų pabaigoje prasidėjo nauja astmos gydymo era, kuri siejama su astmos atsiradimu ir įvedimu į klinikinę praktiką. inhaliuojamųjų gliukokortikosteroidų (ICS).
ICS, gydant astma sergančius pacientus, šiuo metu laikomi pirmos eilės vaistais. Pagrindinis ICS privalumas yra tiesioginis veikliosios medžiagos patekimas į kvėpavimo takus ir didesnės vaisto koncentracijos ten sukūrimas, tuo pačiu pašalinant arba sumažinant sisteminį šalutinį poveikį. Pirmieji ICS astmai gydyti buvo vandenyje tirpaus hidrokortizono ir prednizolono aerozoliai. Tačiau dėl didelio sisteminio ir mažo priešuždegiminio poveikio jų naudojimas buvo neveiksmingas. Aštuntojo dešimtmečio pradžioje. buvo susintetinti lipofiliniai gliukokortikosteroidai, pasižymintys dideliu vietiniu priešuždegiminiu aktyvumu ir silpnu sisteminiu poveikiu. Taigi šiuo metu ICS tapo veiksmingiausiais vaistais pagrindiniam BA gydymui bet kokio amžiaus pacientams (A įrodymų lygis).
IKS gali sumažinti astmos simptomų sunkumą, slopinti alerginio uždegimo aktyvumą, sumažinti bronchų hiperreaktyvumą alergenams ir nespecifiniams dirgikliams (fizinis aktyvumas, šaltas oras, teršalai ir kt.), pagerinti bronchų praeinamumą, pagerinti pacientų gyvenimo kokybę, sumažinti neatvykusių į mokyklą ir darbo skaičių. Įrodyta, kad ICS vartojimas pacientams, sergantiems astma, žymiai sumažina paūmėjimų ir hospitalizacijų skaičių, sumažina mirtingumą nuo astmos, taip pat neleidžia vystytis negrįžtamiems kvėpavimo takų pakitimams (įrodymų lygis A). ICS taip pat sėkmingai naudojami LOPL ir alerginiam rinitui gydyti kaip stipriausi vaistai, turintys priešuždegiminį poveikį.
Skirtingai nuo sisteminių gliukokortikosteroidų, ICS pasižymi dideliu afinitetu receptoriams, mažesnėmis terapinėmis dozėmis ir minimaliu šalutiniu poveikiu.
IKS pranašumas gydant BA prieš kitas priešuždegiminių vaistų grupes nekelia abejonių, o šiandien, pasak daugumos šalies ir užsienio ekspertų, IKS yra veiksmingiausi vaistai BA sergantiems pacientams gydyti. Tačiau net ir gerai ištirtose medicinos srityse yra nepakankamai pagrįstų ir kartais klaidingų idėjų. Iki šiol tebevyksta diskusijos, kaip anksti reikia pradėti gydymą IKS, kokiomis dozėmis, kokiomis IKS ir per kokį švirkštimo aparatą, kaip reikia atlikti ilgalaikę terapiją, o svarbiausia – kaip įsitikinti, kad paskirtas gydymas. ICS terapija nedaro žalos organizmui, tie. Nėra sisteminio ar kitokio šalutinio kortikosteroidų poveikio. Įrodymais pagrįsta medicina kaip tik ir yra skirta kovoti su tokiomis tiek gydytojų, tiek pacientų nuomone egzistuojančiomis tendencijomis, mažinančiomis astmos gydymo ir profilaktikos efektyvumą.
Šiuo metu klinikinėje praktikoje naudojami šie ICS: beklometazono dipropionatas (BDP), budezonidas (BUD), flutikazono propionatas (FP), triamcinolono acetonidas (TAA), flunizolidas (FLU) ir mometazono furoatas (MF). ICS terapijos efektyvumas tiesiogiai priklauso nuo: veikliosios medžiagos, dozės, pristatymo formos ir būdo, atitikimo. gydymo pradžios laikas, gydymo trukmė, astmos sunkumas (paūmėjimas), taip pat LOPL.
Kuris ICS yra efektyvesnis?
Vartojant lygiavertes dozes, visi ICS yra vienodai veiksmingi (įrodymų lygis A). Vaistų farmakokinetiką, taigi ir terapinį efektyvumą, lemia GCS molekulių fizikinės ir cheminės savybės. Kadangi ICS molekulinė struktūra yra skirtinga, jų farmakokinetika ir farmakodinamika skiriasi. IKS klinikiniam efektyvumui ir galimiems šalutiniams poveikiams palyginti siūloma naudoti terapinį indeksą, teigiamo (pageidaujamo) klinikinio ir šalutinio (nepageidaujamo) poveikio santykį, kitaip tariant, IKS efektyvumas vertinamas pagal jų sisteminį poveikį. ir vietinis priešuždegiminis aktyvumas. Esant aukštam terapiniam indeksui, yra geresnis poveikio ir rizikos santykis. Daugelis farmakokinetinių parametrų yra svarbūs nustatant terapinį indeksą. Taigi IKS priešuždegiminį (vietinį) aktyvumą lemia šios vaistų savybės: lipofiliškumas, leidžiantis jiems greičiau ir geriau pasisavinti iš kvėpavimo takų ir ilgiau išsilaikyti kvėpavimo organų audiniuose; afinitetas GCS receptoriams; didelis pirminis inaktyvuojantis poveikis kepenims; ryšio su tikslinėmis ląstelėmis trukmė.
Vienas iš svarbiausių rodiklių yra lipofiliškumas, koreliuojantis su vaisto afinitetu steroidų receptoriams ir jo pusinės eliminacijos periodu. Kuo didesnis lipofiliškumas, tuo vaistas veiksmingesnis, nes jis lengvai prasiskverbia pro ląstelių membranas ir padidina jo kaupimąsi plaučių audinyje. Tai padidina jo veikimo trukmę apskritai ir vietinį priešuždegiminį poveikį, nes susidaro vaisto rezervuaras.
Lipofiliškumas ryškiausias FP, po to seka BDP ir BUD. . FP ir MF yra labai lipofiliniai junginiai, todėl jų pasiskirstymo tūris yra didesnis, palyginti su vaistais, kurie yra mažiau lipofiliški BUD, TAA. BUD yra maždaug 6–8 kartus mažiau lipofilinis nei FP ir atitinkamai 40 kartų mažiau lipofilinis, palyginti su BDP. Tuo pačiu metu daugybė tyrimų parodė, kad mažiau lipofilinis BUD išlieka plaučių audinyje ilgiau nei AF ir BDP. Tai paaiškinama budezonido konjugatų su riebalų rūgštimis lipofiliškumu, kuris yra dešimtis kartų didesnis nei nepažeisto BUD lipofiliškumas, užtikrinantis jo buvimo kvėpavimo takų audiniuose trukmę. Tarpląstelinis BUD esterifikavimas riebalų rūgštimis kvėpavimo takų audiniuose sukelia vietinį susilaikymą ir neaktyvaus, bet lėtai atsinaujinančio laisvo BUD „depo“ susidarymą. Be to, didelis intracelulinis konjuguoto BUD tiekimas ir laipsniškas laisvo BUD išsiskyrimas iš konjuguotos formos gali pailginti receptoriaus prisotinimą ir priešuždegiminį BUD aktyvumą, nepaisant mažesnio afiniteto GCS receptoriams, palyginti su FP ir BDP.
FP turi didžiausią afinitetą GCS receptoriams (maždaug 20 kartų didesnis nei deksametazono, 1,5 karto didesnis nei aktyvaus BDP -17-BMP metabolito ir 2 kartus didesnis nei BUD). Receptorių afiniteto indeksas yra BUD - 235, BDP - 53, FP - 1800. Tačiau, nepaisant to, kad BDP afiniteto indeksas yra žemiausias, jis yra labai efektyvus dėl to, kad patekęs į organizmą virsta monopropionatu, kuris turi afiniteto indeksą 1400. Tai yra, aktyviausi pagal afinitetą GCS receptoriams yra FP ir BDP.
Kaip žinoma, vaisto veiksmingumas vertinamas pagal jo biologinį prieinamumą. ICS biologinį prieinamumą sudaro iš virškinimo trakto absorbuotos dozės biologinis prieinamumas ir iš plaučių absorbuotos dozės biologinis prieinamumas.
Didelis vaisto nusėdimo procentas intrapulmoniniuose kvėpavimo takuose paprastai suteikia geriausią terapinį indeksą tiems ICS, kurių sisteminis biologinis prieinamumas yra mažas dėl absorbcijos iš burnos ertmės ir virškinimo trakto gleivinių. Tai taikoma, pavyzdžiui, BDP, kurios sisteminis biologinis prieinamumas yra dėl absorbcijos žarnyne, priešingai nei BUD, kurio sisteminis biologinis prieinamumas pirmiausia yra dėl absorbcijos per plaučius. Nulinio biologinio prieinamumo (AF) IKS atveju gydymo efektyvumą lemia tik vaistų tiekimo aparato tipas ir inhaliacijos technika, o šie parametrai neturi įtakos terapiniam indeksui.
Kalbant apie ICS metabolizmą, BDP greitai, per 10 minučių, metabolizuojamas kepenyse, susidaro vienas aktyvus metabolitas - 17BMP ir du neaktyvūs - beklometazonas 21-. monopropionatas (21-BMN) ir beklometazonas. FPgreitai ir visiškai inaktyvuojamas kepenyse, susidarant vienam iš dalies aktyviam (1 % FP aktyvumo) metabolitui – 17β-karboksirūgštiui. Budezonidas greitai ir visiškai metabolizuojamas kepenyse dalyvaujant citochromui p450 3A (CYP3A) ir susidaro 2 pagrindiniai metabolitai:6β-hidroksibudezonidas (sudaro abu izomerus) ir16β-hidroksiprednizolonas (sudaro tik 22R). Abu metabolitai turi silpną farmakologinį poveikįskaya veikla.
Palyginti naudotus ICS sunku dėl jų farmakokinetikos ir farmakodinamikos skirtumų. FP yra pranašesnis už kitus ICS visais tirtais farmakokinetikos ir farmakodinamikos parametrais. Naujausių tyrimų rezultatai rodo, kad FP yra mažiausiai 2 kartus veiksmingesnis už BDP ir BUD tomis pačiomis dozėmis.
Neseniai buvo paskelbti 14 lyginamųjų klinikinių AF tyrimų su BDP (7 tyrimai) arba BUD (7 tyrimai) metaanalizės rezultatai. Visuose 14 tyrimų FP buvo skiriama puse (arba mažesnės) dozės, palyginti su BDP arba BUD. Lygindami BDP (400/1600 mcg per parą) ir AF (200/800 mcg per parą) efektyvumą, autoriai nenustatė reikšmingų rytinio maksimalaus iškvėpimo srauto greičio (PEFR) dinamikos skirtumų nė viename iš 7 analizuojami tyrimai. Klinikinis veiksmingumas, taip pat kortizolio koncentracija serume ryte reikšmingai nesiskyrė. Lyginant BUD (400/1600 mcg/d.) ir FP (200/800 mcg/d.) efektyvumą, buvo įrodyta, kad AF statistiškai reikšmingai padidina PEFR reikšmingiau nei BUD. Vartojant mažas vaistų dozes, tarp šių vaistų nėra skirtumo mažinant kortizolio kiekį serume ryte, tačiau, vartojant didesnes vaistų dozes, nustatyta, kad AF šį rodiklį veikia mažiau. Apibendrinant, metaanalizės rezultatai rodo, kad BDP ir pusės dozės FP veiksmingumas yra lygiavertis savo poveikiu PEFR ir klinikiniam veiksmingumui. Pusės dozės FP yra veiksmingesnis už BUD poveikį PEFR. Šie duomenys patvirtina farmakokinetines charakteristikas, santykinį trijų tiriamųjų vaistų afinitetą steroidų receptoriams.
Klinikiniai tyrimai, lyginantys ICS veiksmingumą simptomų ir kvėpavimo funkcijos rodiklių pagerėjimo forma, rodo, kad UD ir BDP aerozoliniuose inhaliatoriuose tomis pačiomis dozėmis efektyvumo praktiškai nesiskiria, FP suteikia tą patį poveikį. ty kaip dviguba BDP arba BUD dozė matuojamame aerozolyje.
Šiuo metu aktyviai tiriamas įvairių IKS lyginamasis klinikinis efektyvumas.
INsICS boro dozė. Apskaičiuota rekomenduojama ar optimali? Kuris efektyvesnis? Atliekant pagrindinį astmos gydymą, siekiant kontroliuoti astmos simptomus, labai domina gydytojai paros IKS dozės ir gydymo trukmės pasirinkimas. Geresnė astmos kontrolė pasiekiama greičiau vartojant didesnes inhaliuojamųjų kortikosteroidų dozes (A įrodymas, 1 lentelė).
Pradinė IKS paros dozė paprastai turi būti 400-1000 mcg (beklometazono atžvilgiu), sergant sunkesnėmis astma gali būti rekomenduojamos didesnės IKS dozės arba pradedamas gydymas sisteminiais kortikosteroidais (C). Standartinės ICS dozės (atitinka 800 mcg beklometazono), jei neveiksmingos, gali būti padidintos iki 2000 mcg beklometazono (A) atžvilgiu.
Duomenys apie su doze susijusį poveikį, pvz., AF, yra įvairūs. Taigi kai kurie autoriai pastebi nuo dozės priklausomą šio vaisto farmakodinaminio poveikio padidėjimą, o kiti mokslininkai nurodo, kad mažų (100 mcg per dieną) ir didelių (1000 mcg per dieną) FP dozių vartojimas yra beveik vienodai efektyvus.
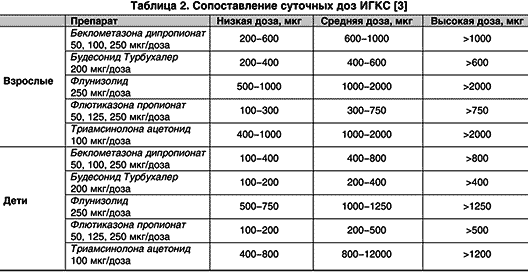
1 lentelė. RApskaičiuotos ekvivalentinės ICS dozės (mcg) A.G. Chuchalin, 2002 m. modifikuotas
| Žemas | Vidutinis | Aukštas | Žemas | Vidutinis | Aukštas | |
| BDP (Beklozon Eco Easy Breathing, Beklat, Beklofort) | 200–500 | 500–1000 | > 1000 | 100- 400 | 400- 800 | > 800 |
| BUD (Budesonidas, Budecort) | 200-400 | 400-800 | > 800 | 100-200 | 200-400 | > 400 |
| FLU* | 500-1000 | 1000 2000 | > 2000 | 500 750 | 1000 1250 | > 1250 |
| FP (flixotide, flochal) | 100-250 | 250-500 | > 500 | 100-200 | 200-500 | > 500 |
| TA* | 400 -1000 | 1000 2000 | > 2000 | 400 800 | 800 1200 | > 1200 |
* veikliosios medžiagos, kurių preparatai neregistruoti Ukrainoje
Tačiau didėjant ICS dozei,sisteminio nepageidaujamo poveikio sunkumą, o vartojant mažas ir vidutines šių vaistų dozespriepuoliai retai sukelia kliniškai reikšmingą skausmąvėlyvos reakcijos į vaistus ir jiems būdingas geras rizikos ir naudos santykis (įrodymų lygis A).
Įrodyta, kad ICS yra labai veiksmingas, kai vartojamas 2 kartus per dieną; vartojant IKS 4 kartus per dieną ta pačia paros doze, gydymo efektyvumas šiek tiek padidėja (A).
Pedersen S. ir kt. parodė, kad mažos IKS dozės sumažina paūmėjimų dažnį ir beta2 agonistų poreikį, pagerina kvėpavimo funkciją, tačiau norint geriau kontroliuoti uždegiminį procesą kvėpavimo takuose ir maksimaliai sumažinti bronchų hiperreaktyvumą, reikalingos didelės šių vaistų dozės.
Dar visai neseniai ICS nebuvo naudojamas astmos paūmėjimams gydyti, nes jie buvo laikomi mažiau veiksmingi paūmėjimo atveju nei sisteminiai kortikosteroidai. Daugybė tyrimų rodo didelį sisteminių kortikosteroidų vartojimo veiksmingumą astmos paūmėjimo metu (įrodymų lygis A). Tačiau nuo praėjusio amžiaus 90-ųjų, kai pasirodė nauji aktyvūs ICS (BUD ir AF), jie buvo pradėti naudoti astmos paūmėjimams gydyti. Daugybė klinikinių tyrimų įrodė, kad ICS BUD ir FP veiksmingumas didelėmis dozėmis per trumpą kursą (2–3 savaites) nesiskiria nuo deksametazono veiksmingumo gydant lengvą ir sunkų astmos paūmėjimą. Inhaliuojamųjų kortikosteroidų vartojimas astmos paūmėjimo metu leidžia normalizuoti pacientų klinikinę būklę ir kvėpavimo funkcijos rodiklius, nesukeliant sisteminio šalutinio poveikio.
Dauguma tyrimų parodė vidutinį ICS veiksmingumą gydant astmos paūmėjimus, kurie svyravo nuo 50 iki 70%, kai buvo vartojama dviguba AF dozė (nuo pagrindinės terapijos dozės), ir padidėjo gydymo veiksmingumas papildomai vartoti ilgai veikiančio beta 2 agonisto salmeterolio 10–15 %. Remiantis tarptautinio konsensuso rekomendacijomis dėl bronchinės astmos gydymo, alternatyva vaisto dozės didinimui, jei neįmanoma užtikrinti optimalios astmos kontrolės naudojant mažų ir vidutinių dozių IKS, yra ilgo veikimo b. agonistai.
Sustiprėjęs ICS, vartojamo kartu su ilgai veikiančiais beta2 adrenerginių receptorių agonistais, poveikis pacientams, sergantiems LOPL, buvo įrodytas atsitiktinių imčių, kontroliuojamu, dvigubai aklu tyrimu TRISTAN (Inhaliuojamųjų steroidų ir ilgo veikimo beta2 agonistų tyrimas), kuriame dalyvavo 1465 pacientai. Taikant kombinuotą gydymą (FP 500 mcg + salmeterolis 50 mcg 2 kartus per dieną), LOPL paūmėjimų dažnis sumažėjo 25%, palyginti su placebu. Kombinuotas gydymas suteikė ryškesnį poveikį pacientams, sergantiems sunkia LOPL, kuriems kurių pradinis FEV1 buvo mažesnis nei 50 % tikėtino th.
Vaistų, vartojamų nuo astmos, veiksmingumas labai priklauso nuo pristatymo būdų , kuris turi įtakos vaisto nusėdimui kvėpavimo takuose. Vaistų nusėdimas plaučiuose, naudojant įvairias tiekimo sistemas, svyruoja nuo 4 iki 60% suvartotos dozės. Yra aiškus ryšys tarp nusėdimo plaučiuose ir klinikinio vaisto poveikio. 1956 m. klinikinėje praktikoje pradėti naudoti dozuoti aerozoliniai inhaliatoriai (MDI) yra labiausiai paplitę inhaliaciniai prietaisai. Naudojant MDI, maždaug 10-30 % vaisto (inhaliuojant be tarpiklio) patenka į plaučius, o vėliau į sisteminę kraujotaką. Didžioji dalis vaisto, ty maždaug 70-80%, nusėda burnos ertmėje ir gerklose ir nuryjama. Klaidos vartojant MDI pasiekia 60%, lemia nepakankamą vaisto patekimą į kvėpavimo takus ir dėl to sumažėja ICS terapijos efektyvumas. Naudojant tarpiklį galima iki 10% sumažinti vaisto pasiskirstymą burnos ertmėje ir optimizuoti veikliosios medžiagos patekimą į kvėpavimo takus, nes nereikalauja absoliutaus paciento veiksmų koordinavimo.
Kuo sunkesnė paciento astma, tuo mažiau veiksmingas gydymas įprastiniais dozuojančiais aerozoliais, nes tik 20-40% pacientų gali atkurti teisingą įkvėpimo techniką juos naudodami. Šiuo atžvilgiu neseniai buvo sukurti nauji inhaliatoriai, kurie nereikalauja paciento judesių koordinavimo įkvėpimo metu. Šiuose įvedimo įtaisuose vaisto tiekimas suaktyvinamas pacientui įkvepiant, tai yra vadinamasis BOI (Breathe Operated Inhaler) – iškvėpimu įjungiamas inhaliatorius. Tai apima „Easi-Breath“ inhaliatorių („lengvas kvėpavimas“). Šiuo metu „Beclazon Eco Easy Breathing“ registruota Ukrainoje. Sausų miltelių inhaliatoriai (dipihaler (Flochal, Budecort), diskiniai (Flixotide (FP), Seretide - FP + salmeterolis), purkštuvai yra tiekimo prietaisai, užtikrinantys optimalią ICS dozę ir sumažinantys nepageidaujamą šalutinį terapijos poveikį. BUD, vartojamas per Turbuhaler, turi tą patį. poveikis , kaip dviguba BUD dozė dozuotame aerozolyje.
Anksti pradėtas priešuždegiminis gydymas IKS sumažina negrįžtamų pakitimų kvėpavimo takuose riziką ir pagerina astmos eigą. Pavėluotai pradėjus gydymą ICS, funkcinių testų rezultatai sumažėja (įrodymų lygis: C).
Atsitiktinių imčių, dvigubai aklas, placebu kontroliuojamas tyrimas START (Inhaled Steroid Treatment as Regular Therapy in Early Asthma Study) parodė, kad kuo anksčiau pradėtas pagrindinis gydymas ICS nuo astmos, tuo liga progresuoja švelniau. START rezultatai buvo paskelbti 2003 m. Ankstyvosios BUD terapijos efektyvumą patvirtino kvėpavimo funkcijos rodiklių padidėjimas.
Ilgalaikis gydymas ICS pagerina arba normalizuoja plaučių funkciją, sumažina kasdienius didžiausio iškvėpimo srauto svyravimus, bronchus plečiančių vaistų ir kortikosteroidų poreikį sisteminiam vartojimui iki visiško jų panaikinimo. Be to, ilgai vartojant vaistus, sumažėja paūmėjimų, hospitalizacijų ir pacientų mirtingumas.
Npageidaujamas IKS poveikis arba gydymo saugumas
Nepaisant to, kad IKS lokaliai veikia kvėpavimo takus, yra prieštaringos informacijos apie neigiamo sisteminio IKS poveikio pasireiškimą – nuo jų nebuvimo iki ryškių apraiškų, keliančių pavojų pacientams, ypač vaikams. Šios NE apima antinksčių žievės funkcijos slopinimą, poveikį kaulų metabolizmui, mėlynių atsiradimą ir odos plonėjimą, burnos kandidozė ir kataraktos susidarymą.
Įtikinamai įrodyta, kad ilgalaikis gydymas IKS nesukelia reikšmingų kaulinio audinio struktūros pokyčių, neveikia lipidų apykaitos, imuninės sistemos būklės, nedidina subkapsulinės kataraktos išsivystymo rizikos. Tačiau klausimai dėl galimo ICS poveikio vaikų linijiniam augimo greičiui ir pagumburio-hipofizės-antinksčių (HPA) ašies būklei ir toliau aptariami.
Sisteminio poveikio pasireiškimus daugiausia lemia vaisto farmakokinetika ir jie priklauso nuo bendro tiekiamų kortikosteroidų kiekio. į sisteminę kraujotaką (sisteminis biologinis prieinamumas)ir GCS klirensas. Todėl pagrindinis veiksnys, lemiantis ICS veiksmingumą ir saugumą, yra vaisto selektyvumassantykis su kvėpavimo takais – aukšto buvimasmažas vietinis priešuždegiminis aktyvumas ir mažas sisteminis aktyvumas (2 lentelė).
2 lentelė . IKS selektyvumas ir sisteminis IKS aktyvumas
| ICS | Vietinė veikla | Sistemos veikla | Vietinio/sisteminio aktyvumo santykis |
| BUD | 1,0 | 1,0 | 1,0 |
| BDP | 0,4 | 3,5 | 0,1 |
| GRIPAS | 0,7 | 12,8 | 0,05 |
| TAA | 0,3 | 5,8 | 0,05 |
ICS saugumą daugiausia lemiaTaip yra dėl jo biologinio prieinamumo iš virškinimo trakto ir yra atvirkščiai proporcinga jam. PeĮvairių ICS peroralinis biologinis prieinamumas svyruoja nuo mažiau nei 1% iki 23%. PirminisNaudojant tarpiklį ir burnos skalavimą po įkvėpimo žymiai sumažėja burnos biologinis prieinamumasPrieinamumas (įrodymų lygis B). Oralinis biologinis prieinamumas yra beveik nulis AF atveju ir 6–13% BUD, o ICS biologinis prieinamumas įkvėpus yra lygus.svyruoja nuo 20 (FP) iki 39% (FLU).
Sisteminis ICS biologinis prieinamumas yra įkvėpto ir geriamojo biologinio prieinamumo suma. BDP sisteminis biologinis prieinamumas yra maždaug 62%, o tai yra šiek tiek didesnis nei kitų ICS.
ICS klirensas yra greitas, jo reikšmė maždaug sutampa su kepenų kraujotakos verte, ir tai yra viena iš minimalių sisteminio NE pasireiškimų priežasčių. ICS patenka į sisteminę kraujotaką po to, kai praeina per kepenis, daugiausia neaktyvių metabolitų pavidalu, išskyrus aktyvų BDP metabolitą - beklometazono 17-monopropionatą (17-BMP) (apie 26%) ir tik mažą dalį. (nuo 23% TAA iki mažiau nei 1% FP) - nepakitusio vaisto pavidalu. Pirmojo praėjimo per kepenis metu inaktyvuojami maždaug 99% FP ir MF, 90% BUD, 80-90% TAA ir 60-70% BDP. Didelis naujų ICS metabolinis aktyvumas (FP ir MF, pagrindinė frakcija, užtikrinanti jų sisteminį aktyvumą, yra ne daugiau kaip 20 % suvartotos dozės (paprastai neviršija 750–1000 µg per dieną)) gali paaiškinti jų geresnį saugumo profilį, palyginti su. į kitus IKS, o kliniškai reikšmingų nepageidaujamų vaistų reiškinių atsiradimo tikimybė yra itin maža, o jei tokių yra, jie dažniausiai būna lengvi ir gydymo nutraukti nereikia.
Visi išvardyti sisteminiai ICS poveikiai yra jų, kaip GCS receptorių agonistų, gebėjimo paveikti hormonų reguliavimą HPA ašyje pasekmė. Todėl gydytojų ir pacientų susirūpinimas dėl ICS vartojimo gali būti visiškai pagrįstas. Tuo pačiu metu kai kurie tyrimai neparodė reikšmingo ICS poveikio HPA ašiai.
Didelis susidomėjimas yra MF, naujas ICS, pasižymintis labai dideliu priešuždegiminiu aktyvumu, kuriam trūksta biologinio prieinamumo. Ukrainoje jį atstovauja tik Nasonex nosies purškalas.
Kai kurie tipiniai kortikosteroidų poveikiai niekada nebuvo pastebėti vartojant inhaliuojamus kortikosteroidus, pvz., susiję su šios klasės vaistų imunosupresinėmis savybėmis arba su subkapsulinės kataraktos išsivystymu.
3 lentelė. SUlyginamieji IKS tyrimai, kurie apėmė gydomojo poveikio nustatymąĮTaktyvumą ir sisteminį aktyvumą, pagrįstą pradiniu kortizolio kiekiu serume arba AKTH analogo stimuliacijos testu.
| Pacientų skaičius | ICS / paros dozė mkg dviejų vaistų | Efektyvumas (rytinis PEF*) | Sistemos veikla |
| 672 suaugusieji | FP/100, 200, 400, 800 iBDP/400 | FP 200 = BDP 400 | FP 400 = BDP 400 |
| 36 suaugusieji | BDP/1500 ir BUD/1600 | BDP = BUD | BDP = BUD – jokio poveikio |
| 398 vaikai | BDP/400 ir FP/200 | FP > BDP | FP = BDP – jokio poveikio |
| 30 suaugusiųjų | BDP/400 ir BUD/400 | BDP = BUD | BDP = BUD – jokio poveikio |
| 28 suaugusieji | BDP/1500 ir BUD/1600 | BDP = BUD | BDP = BUD |
| 154 suaugusieji | BDP/2000 ir FP/1000 | FP = BDP | BDP > FP |
| 585 suaugusieji | BDP/1000 ir FP/500 | FP = BDP | FP = BDP – jokio poveikio |
| 274 suaugusieji | BDP/1500 ir FP/1500 | FP > BDP | BDP = AF – jokio poveikio |
| 261 suaugęs žmogus | BDP/400 ir FP/200 | FP = BDP | BDP > FP |
| 671 suaugęs žmogus | BUD/1600 ir FP/1000,2000 | FP 1000 > BUD, FP 2000 > BUD | FP 1000 = BUD, FP 2000 > BUD |
| 134 suaugusieji | BDP/1600 ir FP/2000 | FP = BDP | FP > BDP |
| 518 suaugusiųjų | BUD/1600 ir FP/800 | FP > BUD | BUD > FP |
| 229 vaikai | BUD/400 ir FP/400 | FP > BUD | BUD > FP |
| 291 suaugęs žmogus | TAA/800 ir FP/500 | FP > TAA | FP = TAA |
| 440 suaugusiųjų | FLU/1000 ir FP/500 | FP > FLU | FP = FLU |
| 227 suaugusieji | BUD/1200 ir FP/500 | BUD = AF | BUD > FP |
Pastaba: * PEF didžiausias iškvėpimo srautas
Sisteminio ICS poveikio priklausomybė nuo dozėsnarkotikų vartojimas nėra akivaizdus, tyrimų rezultatai prieštaringi (3 lentelė). NeŽvelgiant į kylančius klausimus, pateikti klinikiniai atvejai verčia susimąstyti apie saugumąilgalaikio gydymo didelėmis ICS dozėmis pavojus. Tikriausiai yra pacientų, kurie yra labai jautrūs steroidų terapijai. Tikslasdidelės ICS dozės tokiems asmenims gali padidinti sisteminių susirgimų dažnįšalutiniai poveikiai. Veiksniai, lemiantys didelį paciento jautrumą GCS, vis dar nežinomi. Galima tik pastebėti, kad tokių skaičiusPacientų yra labai mažai (4 aprašyti atvejai vienamVien 16 milijonų pacientų per naudojimo metusFP nuo 1993 m.).
Didžiausią susirūpinimą kelia tai, kad ICS gali turėti įtakos vaikų augimui, nes šie vaistai paprastai vartojami ilgą laiką. Vaikų, sergančių astma, negaunančių jokia forma kortikosteroidų, augimą gali įtakoti daugybė veiksnių, tokių kaip: gretutinė atopija, astmos sunkumas, lytis ir kt. Vaikystės astma gali būti susijusi su tam tikru augimo sulėtėjimu, nors dėl to nesumažėja galutinis suaugusiojo ūgis. Dėl daugelio veiksnių, turinčių įtakos astma sergančių vaikų augimui, tyrimai buvo skirti susirūpinęs dėl inhaliuojamųjų kortikosteroidų ar sisteminių kortikosteroidų poveikio augimui,turėti prieštaringų rezultatų.
Vietinis IKS šalutinis poveikis yra: burnos ertmės ir burnos ryklės kandidozė, disfonija, kartais kosulys, atsirandantis dėl viršutinių kvėpavimo takų dirginimo, paradoksinis bronchų spazmas.
Vartojant mažas ICS dozes, vietinio šalutinio poveikio dažnis yra mažas. Taigi, burnos kandidozė pasireiškia 5% pacientų, vartojančių mažas ICS dozes, ir iki 34% pacientų, vartojančių dideles šių vaistų dozes. Disfonija stebima 5-50% pacientų, vartojančių IKS; jo vystymasis taip pat siejamas su didesnėmis vaistų dozėmis. Kai kuriais atvejais, naudojant ICS, gali išsivystyti refleksinis kosulys. Paradoksinis bronchų spazmas gali išsivystyti reaguojant į ICS skyrimą naudojant MDI. Klinikinėje praktikoje bronchus plečiančių vaistų vartojimas dažnai užmaskuoja tokio tipo bronchų susiaurėjimą.
Taigi ICS buvo ir išlieka kertinis vaikų ir suaugusiųjų astmos terapijos akmuo. Ilgalaikio mažų ir vidutinių dozių ICS vartojimo saugumas nekelia abejonių. Ilgai vartojant dideles ICS dozes, gali išsivystyti sisteminiai poveikiai, iš kurių reikšmingiausi yra vaikų CPR sulėtėjimas ir antinksčių funkcijos slopinimas.
Naujausiose tarptautinėse suaugusiųjų ir vaikų astmos gydymo rekomendacijose siūloma skirti kombinuotą terapiją su IKS ir ilgai veikiančiais beta-2 agonistais visais atvejais, kai vartojant mažas IKS dozes efektas nepasiekiamas. Šio metodo pagrįstumą patvirtina ne tik didesnis jo efektyvumas, bet ir geresnis saugos profilis.
Skirti dideles ICS dozes patartina tik tuo atveju, jei kombinuotas gydymas yra neveiksmingas. Ko gero, šiuo atveju sprendimą dėl didelių IKS dozių vartojimo turėtų priimti pulmonologas ar alergologas. Pasiekus klinikinį poveikį, ICS dozę patartina titruoti iki mažiausio veiksmingo. Ilgai gydant astmą didelėmis ICS dozėmis, būtina stebėti saugumą, kuris gali apimti vaikų CPR matavimą ir kortizolio koncentraciją ryte.
Sėkmingos terapijos raktas yra paciento ir gydytojo santykis bei paciento požiūris į gydymą.
Atminkite, kad tai yra bendras nustatymas. Neatmetamas individualus požiūris į astma sergančių pacientų gydymą, kai gydytojas pasirenka vaistą, jo vartojimo režimą ir dozę. Jeigu gydytojas, remdamasis sutarčių dėl astmos gydymo rekomendacijomis, vadovaujasi savo žiniomis, turima informacija ir asmenine patirtimi, tuomet gydymo sėkmė garantuota.
LITERATŪRA
1. Pasaulinė astmos valdymo ir prevencijos strategija. Nacionaliniai sveikatos institutai, Nacionalinis širdies, plaučių ir kraujo institutas. Peržiūrėta 2005 m. NIH leidinio Nr. 02-3659 // www.ginasthma.com m. Barnesas PJ. Inhaliuojamųjų kortikosteroidų veiksmingumas sergant astma. J Allergy Clin Immunol 1998; 102 (4 pt 1): 531-8.
2. Barnes N.C., Hallet C., Harris A. Klinikinė flutikazono propionato patirtis sergant astma: veiksmingumo ir sisteminio aktyvumo metaanalizė, palyginti su budezonidu ir beklometazono dipropionatu, kai dozė yra pusė mikrogramo ar mažesnė. Respira. Med., 1998; 92:95.104.
3. Pauwels R, Pedersen S, Busse W ir kt. Ankstyva intervencija su budezonidu sergant lengva nuolatine astma: atsitiktinių imčių, dvigubai aklas tyrimas. Lancet 2003;361:1071-76.
4. Pagrindinės EPR-2 ekspertų grupės ataskaitos nuostatos: pagrindinės bronchinės astmos diagnostikos ir gydymo tendencijos. Nacionalinis širdies, plaučių ir kraujo institutas. NIH leidinys N 97-4051A. 1997 m. gegužės mėn. / Vertimas. Redaguota A.N. Tsoi. M., 1998 m.
5. Crocker IC, Church MK, Newton S, Townley RG. Gliukokortikoidai slopina proliferaciją ir interleukino 4 bei interleukino 5 sekreciją aeroalergenams specifinėmis 2 tipo T pagalbininkų ląstelių linijomis. Ann Allergy Asthma Immunol, 1998;80:509-16.
6. Umland SP, Nahrebne DK, Razac S ir kt. Vietiškai aktyvių gliukokortikoidų slopinamasis poveikis IL4, IL5 ir gama interferono gamybai kultivuojamose pirminėse CD4+ T ląstelėse. J. Allergy Clin. Immunol 1997; 100: 511-19.
7. Derendorf H. Inhaliuojamųjų kortikosteroidų farmakokinetika ir farmakodinaminės savybės veiksmingumo ir saugumo. Respir Med 1997; 91 (priedas A): 22-28.
8. Johnson M. Inhaliuojamųjų gliukokortikoidų farmakodinamika ir farmakokinetika. J Allergy Clin Immunol 1996;97:169-76.
9. Brokbank W, Brebner H, Pengelly CDR. Lėtinė astma gydoma aerozoliniu hidrokortizonu. Lancetas 1956:807.
10. Vaikų astmos valdymo programos tyrimo grupė. Ilgalaikis budezonido arba nedokromilo poveikis astma sergantiems vaikams // N. Engl. J.Med. – 2000. – T. 343. – P. 1054-1063.
11. Suissa S, Ernst P. // J Allergy Clin Immunol.-2001.-Tol 107, N 6.-P.937-944.
12. Suissa S., Ernst P., Benayoun S. ir kt. // N Engl J Med.-2000.-T. 343, N 5.-P.332. Lipworthas B.J., Jacksonas C.M. Inhaliuojamųjų ir intranazalinių kortikosteroidų saugumas: pamokos naujajam tūkstantmečiui // Vaistų sauga. – 2000. – T. 23. – P. 11–33.
13. Smolenovas I.V. Inhaliuojamųjų gliukokortikosteroidų saugumas: nauji atsakymai į senus klausimus // Atmosfera. Pulmonologija ir alergologija. 2002. Nr.3. – 10-14 p.
14. Burge P, Calverley P, Jones P ir kt. Atsitiktinis, dvigubas, placebu kontroliuojamas flutikazono propionato tyrimas pacientams, sergantiems vidutinio sunkumo ar sunkiomis lėtinėmis obstrukcinėmis plaučių ligomis: ISOLDE tyrimas. BMJ 2000;320:1297-303.
15. Sutochnikova O.A., Chernyaev A.L., Chuchalin A.G. Inhaliuojami gliukokortikosteroidai gydant bronchinę astmą // Pulmonologija. – 1995 m. – 5 tomas. – P. 78 – 83.
16. Allen D.B., Mullen M., Mullen B. Geriamųjų ir inhaliuojamųjų kortikosteroidų poveikio augimui metaanalizė // J. Allergy Clin. Immunol. – 1994. – T. 93. – P. 967-976.
17. Hogger P, Ravert J, Rohdewald P. Inhaliuojamų gliukokortikoidų tirpimas, audinių surišimas ir receptorių surišimo kinetika. Eur Respir J 1993;6(suppl.17):584S.
18. Tsoi A.N. Šiuolaikinių inhaliuojamųjų glikokortikosteroidų farmakokinetiniai parametrai // Pulmonologija. 1999. Nr 2. P. 73-79.
19. Miller-Larsson A., Maltson R. H., Hjertberg E. ir kt.. Grįžtamoji budezonido riebalų rūgščių konjugacija: naujas mechanizmas, skirtas ilgalaikiam lokaliai vartojamo steroido susilaikymui kvėpavimo takų audinyje // Drug.metabol. Dispos. 1998 m.; v. 26 N 7: 623-630.A. K., Sjodin, Hallstrom G. Budezonido, gliukokortikoido nuo astmos, riebalų rūgščių esterių grįžtamasis susidarymas žmogaus plaučių ir kepenų mikrosomose // Vaistas. Metabolinis. Dispos. 1997 m.; 25: 1311-1317.
20. Van den Bosch J. M., Westermann C. J. J., Edsbacker J. ir kt. Ryšys tarp plaučių audinio ir įkvepiamo budezonido koncentracijos kraujo plazmoje // Biopharm Drug. Dispos. 1993 m.; 14:455-459.
21. Wieslander E., Delander E. L., Jarkelid L. ir kt.. Budezonido grįžtamosios riebalų rūgščių konjugacijos farmakologinė svarba žiurkės ląstelių linijoje in vitro // Am. J. Respira. Ląstelė. Mol. Biol. 1998;19:1-9.
22. Thorsson L., Edsbacker S. Conradson T. B. Budezonido nusėdimas plaučiuose iš Turbuhaler yra dvigubai didesnis nei iš slėginio dozuoto inhaliatoriaus p-MDI // Eur. Respira. J. 1994; 10: 1839-1844
23. Derendorf H. Inhaliuojamųjų kortikosteroidų farmakokinetinės ir farmakodinaminės savybės, susijusios su veiksmingumu ir saugumu // Respir. Med. 1997 m.; 91 (A priedas): 22-28
24. Jackson W. F. Nebulized Budesonide Therapy astmos mokslinė ir praktinė apžvalga. Oxford, 1995: 1-64
25. Trescoli-Serrano C., Ward W. J., Garcia-Zarco M. ir kt. Inhaliuojamo budezonido ir beklometazono absorbcija iš virškinimo trakto: ar tai reikšmingas sisteminis poveikis? //Esu. J. Respira. Krit. Care Med. 1995 m.; 151 (Nr. 4, 2 dalis):A. Borgstrom L. E., Derom E., Stahl E. ir kt. Inhaliacinis prietaisas daro įtaką terbutalino nusėdimui plaučiuose ir bronchus plečiančiam poveikiui //Am. J. Respira. Krit. Care Med. 1996 m.; 153: 1636-1640.
26. Ayresas J.G., Batemanas E.D., Lundbackas E., Harrisas T.A.J. Didelė flutikazono propionato dozė, 1 mg per parą, palyginti su flutikazono propionatu, 2 mg per parą, arba budezonido, 1,6 mg per parą, pacientams, sergantiems lėtine sunkia astma // Eur. Respira. J. – 1995. – T.8(4). – P. 579-586.
27. Boe J., Bakke P., Rodolen T. ir kt. Didelės inhaliuojamųjų steroidų dozės astmatikams: vidutinio veiksmingumo padidėjimas ir pagumburio hipofizės-antinksčių (HPA) ašies slopinimas // Eur. Respira. J. –1994 m. – t. 7. – P. 2179-2184.
28. Dahl R., Lundback E., Malo J.L. ir kt. Flutikazono propionato dozės nustatymo tyrimas suaugusiems pacientams, sergantiems vidutinio sunkumo astma // Krūtinė. – 1993. – T. 104. – P. 1352-1358.
29. Daley-Yates P.T., Price A.C., Sisson J.R. et al. Beklometazono dipropionatas: absoliutus biologinis prieinamumas, farmakokinetika ir metabolizmas po intraveninio, peroralinio, intranazalinio ir įkvėpimo vartojimo žmogui // J. Clin. Pharmacol. – 2001. – T. 51. – P. 400-409.
30. Mollmann H., Wagner M., Meibohm B. ir kt., Farmakokinetinė ir farmakodinaminė raida flutikazono propionato įkvėpuscija // Eur. J. Clin. Pharmacol. – 1999. – T. 53. – P. 459–467.
31. Ninanas T.K., Russell G. Astma, gydymas inhaliaciniais kortikosteroidais ir augimas // Arch. Dis. Vaikas. – 1992 m. – t. 67 straipsnio 6 dalį. – P. 703 705.
32. Pedersen S., Byrne P. O. Inhaliuojamųjų kortikosteroidų veiksmingumo ir saugumo palyginimas sergant astma // Eur. J. Alergija. Clin. Immunol. – 1997. – V.52 (39). – P.1-34
33. Thompson P. I. Vaistų pristatymas į mažus kvėpavimo takus // Amer. J. Repir. Krit. Med. – 1998. – V. 157. – P.199 – 202.
34. Boker J., McTavish D., Budesonide. Atnaujinta jo farmakologinių savybių apžvalga ir terapinis veiksmingumas sergant astma ir rinitu // Narkotikai. – 1992 m. – v. 44. – Nr.3. – 375 – 407.
35. Calverley P, Pauwels R, Vestibo J ir kt. Kombinuotas salmeterolis ir flutikazonas gydant lėtinę obstrukcinę plaučių ligą: atsitiktinių imčių kontroliuojamas tyrimas. Lancet 2003;361:449-56.
36. Kvėpavimo takų uždegimo įvertinimas sergant astma / A.M. Vignola. J. Bousquet, P. Chanez ir kt. //Esu. J. Respira. Krit. Care Med. – 1998. – V. 157. – P. 184–187.
37. Yashina L.O., Gogunska I.V. Inhaliuojamųjų kortikosteroidų veiksmingumas ir saugumas gydant bronchinę astmą // Astma ir alergijos. – 2002. Nr.2. – P. 21 – 26.
38. Inhaliuojamųjų kortikosteroidų veiksmingumas ir saugumas kontroliuojant ūminius astmos priepuolius vaikams, kurie buvo gydomi skubios pagalbos skyriuje: kontroliuojamas lyginamasis tyrimas su geriamuoju prednizolonu / B. Volovits, B. Bentur, Y. Finkelshtein ir kt. // J. Alergijos klinika. Immunol. – 1998. – V. 102. – N. 4. – P.605 – 609.
39. Sinopalnikovas A.I., Klyachkina I.L. Vaistų tiekimo į kvėpavimo takus nuo bronchinės astmos priemonės // Rusijos medicinos žinios. -2003 m. Nr.1. 15-21 p.
40. Nicklas RA. Paradoksalus bronchų spazmas, susijęs su inhaliuojamųjų beta agonistų vartojimu. J Allergy Clin Immunol 1990;85:959-64.
41. Pedersen S. Astma: pagrindiniai mechanizmai ir klinikinis valdymas. Red. P. J. Barnesas. Londonas 1992, p. 701-722
42. Ebden P., Jenkins A., Houston G. ir kt. Dviejų didelių dozių kortikosteroidų aerozolių, beklometazono dipropionato (1500 mikrogramų per dieną) ir budezonido (1600 mikrogramų per dieną), palyginimas lėtinei astmai gydyti // Krūtinė. – 1986. – T. 41. – P.869-874.
43. Brown P.H., Matusiewicz S.P., Shearing C. ir kt. Sisteminis didelės dozės inhaliuojamų steroidų poveikis: beklometazono dipropionato ir budezonido palyginimas sveikiems asmenims // Krūtinė. – 1993.– T. 48. – P. 967-973.
44. Inhaliuojamųjų ir intranazalinių kortikosteroidų saugumas: nauda naujajam tūkstantmečiui // Vaistų sauga. – 2000. – t. 23. – P. 11–33.
45. Doull I.J.M., Freezer N.J., Holgate S.T. Vaikų iki brendimo, sergančių lengva astma, gydytų inhaliuojamuoju beklometazono dipropionatu, augimas // Am. J.Respira. Krit. Care Med. – 1995. – T. 151. – P.1715-1719.
46. Goldstein D.E., Konig P. Įkvėpto beklometazono dipropionato poveikis hipotalaminės hipofizės-antinksčių ašies funkcijai astma sergantiems vaikams // Pediatrics. – 1983. – T. 72. – P. 60-64.
47. Kamada A.K., Szefler S.J. Gliukokortikoidai ir astma sergančių vaikų augimas // Pediatr. Alergija Immunol. – 1995. – T. 6. – P. 145-154.
48. Prahl P., Jensen T., Bjerregaard-Andersen H. Antinksčių žievės funkcija vaikams, gydomiems didelėmis steroidų aerozolių dozėmis // Alergija. – 1987. – T.42. – P. 541-544.
49. Priftis K., Milner A.D., Conway E., Honor J.W. Antinksčių funkcija sergant astma // Arch. Dis. Vaikas. – 1990 m. – t. 65. – P. 838-840.
50. Balfour-Lynn L. Augimas ir vaikystės astma // Arch. Dis. Vaikas. – 1986. – T. 61 straipsnio 11 dalį. – P. 1049-1055.
51. Kannisto S., Korppi M., Remes K., Voutilainen R. Antinksčių slopinimas, įvertintas mažos dozės adrenokortikotropino testu, ir astma sergančių vaikų, gydomų inhaliuojamais steroidais, augimas // Klinikinės endokrinologijos ir metabolizmo žurnalas. – 2000. – T. 85. – P. 652 – 657.
52. Prahl P. Antinksčių žievės slopinimas po gydymo beklometazono dipropionatu ir budezonidu // Clin. Exp. Alergija. – 1991. – T. 21.– P. 145-146.
53. Tabachnik E., Zadik Z. Dienos kortizolio sekrecija gydant inhaliuojamuoju beklometazono dipropionatu astma sergantiems vaikams // J. Pediatr. – 1991 m. – t. 118. – P. 294-297.
54. Capewell S., Reynolds S., Shuttleworth D. ir kt. Purpura ir odos retėjimas, susijęs su didelėmis inhaliuojamųjų kortikosteroidų dozėmis // BMJ. – 1990. T.300. – P. 1548-1551.
Pirmasis vietinis inhaliacinis gliukokortikosteroidas buvo sukurtas tik praėjus 30 metų po pačių gliukokortikosteroidų atradimo. Šis vaistas buvo gerai žinomas beklometazono dipropionatas. 1971 metais juo sėkmingai buvo gydomas alerginis rinitas, o 1972 metais – bronchinė astma. Vėliau buvo sukurti kiti įkvepiami hormonai. Šiuo metu vietiniai gliukokortikosteroidai dėl ryškaus priešuždegiminio antialerginio poveikio ir mažo sisteminio aktyvumo yra tapę pirmos eilės vaistais bazinėje bronchinės astmos terapijoje – pagrindiniu gydymu, kuriuo siekiama suvaldyti ligą.
Nuo sisteminių jie skiriasi ne tik vartojimo būdu, bet ir daugybe savybių: lipofiliškumu, mažu absorbcijos į kraują procentu, inaktyvacijos greičiu, trumpu pusinės eliminacijos periodu iš kraujo plazmos. Didelis jų efektyvumas leidžia juos vartoti labai mažomis dozėmis, matuojant mikrogramais, o tik nedidelė inhaliacinės dozės dalis absorbuojama į kraują ir turi sisteminį poveikį. Tokiu atveju vaistas greitai inaktyvuojamas, o tai dar labiau sumažina sisteminių komplikacijų tikimybę. Dėl šių savybių šalutinio poveikio dažnis ir sunkumas, net ir ilgai gydant vietiniais gliukokortikosteroidais, yra daug kartų mažesnis nei gydant sisteminiais hormonais.
Nepaisant to, daugelis pacientų ir net kai kurie gydytojai perkelia į inhaliacinius hormonus tas pačias baimes, kurias sukėlė sisteminė hormonų terapija, ir taip pat painioja sąvokas „ilgalaikė palaikomoji terapija ligų kontrolei“ ir „priklausomybė nuo vaistų“. Kartais tai lemia nepagrįstą būtino gydymo atsisakymą arba pavėluotą tinkamo gydymo pradžią, o tai gali sukelti nekontroliuojamą bronchinės astmos eigą ir gyvybei pavojingų komplikacijų vystymąsi, o jų gydymui reikės vartoti sisteminius hormonus, kurių šalutinis poveikis yra pagrįstas susirūpinimas. Be to, tyrimais įrodyta, kad kuo anksčiau pradedamas bronchinės astmos gydymas, tuo jis veiksmingesnis ir reikės mažiau gydymo, kad liga būtų suvaldyta.
Ilgalaikė nekontroliuojama astmos eiga taip pat sukelia sklerozinių procesų vystymąsi bronchų medyje, dėl kurio gali atsirasti negrįžtama bronchų obstrukcija. Norint to išvengti, būtina ir ankstyva terapija inhaliuojamaisiais hormonais, kurie ne tik sumažina uždegimo aktyvumą bronchų medyje, bet ir slopina fibroblastų dauginimąsi bei aktyvumą, užkertant kelią sklerozinių procesų vystymuisi.
Inhaliuojamieji gliukokortikosteroidai, skirti bronchinei astmai gydyti, vartojant ilgai, normalizuoja plaučių funkciją, mažina didžiausio iškvėpimo srauto svyravimus, neleidžia sumažėti jautrumui beta-2 agonistams, gerina gyvenimo kokybę, mažina paūmėjimų ir hospitalizacijų dažnumą, ir užkirsti kelią negrįžtamos bronchų obstrukcijos vystymuisi. Dėl šios priežasties jie laikomi pirmos eilės vaistais gydant bet kokio sunkumo nuolatinę bronchinę astmą, pradedant nuo lengvos formos.
© Nadežda Knyažeskaja
Nauji straipsniai
- Teatro žaidimų rengimas ir vedimas antroje darželio jaunesniojoje grupėje Teatralinio žaidimo jaunesniojoje grupėje santrauka
- „planas - elementarių matematinių sąvokų formavimo mazgų metmenys parengiamojoje mokyklai grupėje: „kelionė į matematikos šalį
- GCD santrauka vyresniojoje grupėje
- Vidurinės grupės matematinio tobulėjimo edukacinių užsiėmimų santrauka „Suskaičiuokime triušius“
- Kalbos ugdymas per teatro veiklą“ medžiaga (vyresnė grupė) šia tema
- Vaikas ir kelių eismo taisyklių medžiaga tema Vaikas ir eismo taisyklės
- Priešgaisrinės saugos pramogų scenarijus vyresniems ikimokyklinio amžiaus vaikams Darželio saugos scenarijai
- Vaikų ir kelių eismo taisyklių medžiaga tema Situacijos keliuose, kelių eismo taisyklės vaikams
- Socialinis darbuotojas nėra darbas – pašaukimas!
- Kuzbaso valstybinis technikos universitetas pavadintas T
Populiarūs straipsniai
- Profesionalus pokalbis kaip būdas įvertinti būsimą personalą
- „Nenurodytų“ viešojo sektoriaus darbuotojų pajamų didinimas
- Ką daro tekintojas? Turner – kas tai? Profesija tekintojo. Kur galima įsidarbinti tekintoju?
- Profesija „tekininkas“: mokymai, rangai
- Modeliavimas kaip pažinimo modeliavimo ir formalizavimo metodas
- Kritulių pasiskirstymo diagrama programoje „Excel“ Saulėtų dienų diagrama pagal mėnesį
- N ir NN rašyba dalyviuose ir būdvardžiuose
- Kas yra veiksmažodžių morfemos
- Butlerovo teorijos 1 ir 2 pozicijos
- Kas yra alfa skilimas ir beta skilimas?
