Oblike za vdihavanje. Farmakološka skupina - glukokortikosteroidi Inhalacijski glukokortikosteroidi za zdravljenje bronhialne astme
Za navedbo:Knyazheskaya N.P. Glukokortikosteroidi pri zdravljenju bronhialne astme // BC. 2002. št. 5. Str. 245
Oddelek za pulmologijo FUV RSMU
IN v zadnjih letih je prišlo do znatnega napredka pri zdravljenju bronhialna astma (BA)... Očitno je to posledica opredelitve AD kot kronične vnetne bolezni dihal in posledično s široko uporabo inhalacij glukokortikosteroidi (GCS)kot osnovna protivnetna zdravila. Kljub doseženemu napredku pa ravni nadzora nad potekom bolezni ni mogoče šteti za zadovoljivo. Na primer, skoraj vsak tretji bolnik z BA se ponoči vsaj enkrat mesečno zbudi zaradi simptomov bolezni. Več kot polovica bolnikov ima omejeno telesno aktivnost, več kot tretjina jih mora izpustiti šolanje ali biti odsotna z dela. Več kot 40% bolnikov je zaradi poslabšanja bolezni prisiljenih poiskati nujno oskrbo. Razlogi za takšno situacijo so različni, nenazadnje pa pri tem igra tudi premalo zavedanja zdravnika o patogenezi AD in s tem tudi izbira napačne taktike zdravljenja.
Opredelitev in razvrstitev BA Bronhialna astma je kronična bolezen dihalnih poti, pri kateri sodeluje veliko celic: mastociti, eozinofili in T-limfociti. Pri dovzetnih posameznikih se zaradi tega vnetja ponavljajo epizode sopenja, zasoplosti, stiskanja v prsih in kašljanja, zlasti ponoči in / ali zgodaj zjutraj. Te simptome spremlja razširjena, a spremenljiva ovira bronhialnega drevesa, ki je vsaj delno reverzibilna, spontano ali pod vplivom zdravljenja. Vnetje povzroči tudi povečan odziv dihalnih poti na različne dražljaje (hiperodzivnost).
Ključne določbe opredelitve je treba upoštevati naslednje:
1. BA je kronična obstojna vnetna bolezen dihal, ne glede na resnost poteka.
2. Vnetni proces vodi v bronhialno hiperreaktivnost, oviranje in pojav dihalnih simptomov.
3. Obstrukcija dihalnih poti je vsaj delno reverzibilna.
4. Atopija - genetska nagnjenost k proizvodnji imunoglobulinov razreda E (morda niso vedno prisotni).
Bronhialno astmo lahko razvrstimo na podlagi etiologije, resnosti poteka in značilnosti manifestacije bronhialne obstrukcije.
Vendar je trenutno treba bronhialno astmo najprej razvrstiti glede na njeno resnost, saj to odraža resnost vnetnega procesa v dihalnih poteh in določa taktiko protivnetnega zdravljenja.
Resnostdoločajo naslednji kazalniki:
- Število nočnih simptomov na teden.
- Število dnevnih simptomov na dan in na teden.
- Frekvenca uporabe kratko delujočih b 2 -agonistov.
- Resnost telesne aktivnosti in motenj spanja.
- Najvišje vrednosti izdihanega pretoka (PEF) in njegov odstotek z želeno ali najboljšo vrednostjo.
- Dnevna nihanja PSV.
- Obseg terapije.
Obstaja 5 stopinj resnosti BA: blago občasno; lahka obstojnost; zmerno vztrajen; hudo vztrajno; hudo obstojno odvisno od steroidov (tabela 1).
BA prekinitvenega toka: simptomi astme manj kot 1-krat na teden; kratka poslabšanja (od nekaj ur do več dni). Nočni simptomi 2-krat na mesec ali manj; brez poslabšanj brez simptomov in normalnega delovanja pljuč: najvišji pretok izdiha (PEF)\u003e 80% pričakovanega in nihanja PEF manj kot 20%.Vztrajno blago BA. Simptomi enkrat na teden ali pogosteje, vendar manj pogosto kot enkrat na dan. Poslabšanje bolezni lahko moti aktivnost in spanje. Nočni simptomi se pojavijo več kot 2-krat na mesec. PSV več kot 80% zapadlosti; Nihanja PSV so 20-30%.
Zmerna astma... Dnevni simptomi. Poslabšanja motijo \u200b\u200baktivnost in spanje. Nočni simptomi se pojavijo več kot enkrat na teden. Dnevni vnos kratko delujočih b 2 -agonistov. PSV 60-80% zapadlosti. Nihanja PSV so več kot 30%.
Huda BA: stalni simptomi, pogosta poslabšanja, pogosti nočni simptomi, telesna aktivnost je omejena z manifestacijami astme. PSV manj kot 60% zapadlosti; nihanja nad 30%.
Opozoriti je treba, da je resnost astme po teh kazalcih mogoče le pred začetkom zdravljenja. Če bolnik že prejema potrebno terapijo, je treba upoštevati tudi njegovo količino. Torej, če ima bolnik glede na klinično sliko blago vztrajno astmo, hkrati pa prejme zdravila, ki ustrezajo hudi vztrajni astmi, je temu bolniku diagnosticirana huda astma.
Huda BA, odvisna od steroidov: ne glede na klinično sliko je treba bolnika, ki se dolgotrajno zdravi s sistemskimi kortikosteroidi, obravnavati kot bolnika s hudo BA.
Vdihnjen GCS Priporočeno postopni pristop k terapiji astmeodvisno od resnosti poteka (tabela 1). Vsa zdravila za zdravljenje astme so razdeljena v dve glavni skupini: za dolgoročno obvladovanje vnetnega procesa in zdravila za lajšanje akutnih simptomov astme. Osnova terapije za dolgoročno kontrolo vnetnega procesa so inhalacijski glukokortikosteroidi (ICS), ki jih je treba uporabljati od druge stopnje (blag vztrajen potek) do pete (hudo od steroidov odvisen potek). Zato se ICS trenutno šteje za prvo linijo zdravljenja astme. Višja kot je resnost astme, uporabiti je treba večje odmerke ICS. Po številnih študijah so imeli bolniki, ki so začeli zdravljenje z ICS najpozneje dve leti od začetka bolezni, pomembne prednosti pri izboljšanju nadzora simptomov astme v primerjavi s skupino, ki je začela zdravljenje z ICS po več kot 5 letih od začetka bolezni.
Mehanizmi delovanja in farmakokinetika
ICS se lahko vežejo na določene receptorje v citoplazmi, jih aktivirajo in z njimi tvorijo kompleks, ki se nato dimerizira in premakne v celično jedro, kjer se veže na DNA in sodeluje z mehanizmi transkripcije ključnih encimov, receptorjev in drugih kompleksnih beljakovin. To vodi do manifestacije farmakološkega in terapevtskega delovanja.
Protivnetni učinek ICS je povezan z njihovim zaviralnim učinkom na vnetne celice in njihove mediatorje, vključno s proizvodnjo citokinov, motenjem presnove arahidonske kisline in sintezo levkotrienov in prostaglandinov, preprečevanjem migracije in aktivacijo vnetnih celic. ICS z zaviranjem interlevkina-5 poveča sintezo protivnetnih beljakovin (lipokortin-1), poveča apoptozo in zmanjša število eozinofilcev. Tako ICS vodijo k stabilizaciji celičnih membran, zmanjšujejo vaskularno prepustnost, izboljšujejo funkcijo β-receptorjev tako s sintezo novih kot tudi s povečanjem njihove občutljivosti in spodbujajo epitelijske celice.
ICS se od sistemskih glukokortikosteroidov razlikujejo po svojih farmakoloških lastnostih: lipofilnosti, hitri inaktivaciji in kratkem razpolovnem času iz krvne plazme. Pomembno je upoštevati, da je zdravljenje z ICS lokalno (lokalno), ki zagotavlja izrazite protivnetne učinke neposredno na bronhialno drevo z minimalnimi sistemskimi manifestacijami. Količina ICS, ki se dovaja v dihala, je odvisna od nominalnega odmerka zdravila, vrste inhalatorja, prisotnosti ali odsotnosti pogonskega goriva in tehnike vdihavanja. Do 80% bolnikov ima težave z uporabo merjenih aerosolov.
Najpomembnejša značilnost manifestacije selektivnosti in časa zadrževanja zdravila v tkivih je lipofilnost... Zaradi njihove lipofilnosti se ICS kopičijo v dihalnih poteh, njihovo sproščanje iz tkiv se upočasni in poveča njihova afiniteta za glukokortikoidni receptor. Visoko lipofilni ICS se hitreje in bolje zajame iz lumna bronhijev in se dolgo zadrži v tkivih dihal. ICS se od sistemskih zdravil razlikuje po lokalnem (lokalnem) delovanju. Zato je neuporabno predpisovati inhalacijo sistemskih kortikosteroidov (hidrokortizon, prednizolon in deksametazon): ta zdravila imajo ne glede na način uporabe le sistemski učinek.
Številne randomizirane s placebom nadzorovane študije pri bolnikih z BA so pokazale učinkovitost vseh odmerkov ICS v primerjavi s placebom.
Sistemsko biološka uporabnostje sestavljen iz peroralnega in inhalacijskega. Od 20 do 40% vdihanega odmerka zdravila vstopi v dihala (ta vrednost se znatno razlikuje glede na napravo za dajanje in pacientovo tehniko vdihavanja). Biološka uporabnost v pljučih je odvisna od odstotka zdravila, ki vstopi v pljuča, prisotnosti ali odsotnosti nosilca (najboljši kazalniki imajo inhalatorji, ki ne vsebujejo freona) in od absorpcije zdravila v dihalih. 60-80% inhalacijskega odmerka se odloži v orofarinksu in se pogoltne, nato pa se v prebavilih in jetrih v celoti ali delno presnovi. Peroralna razpoložljivost je odvisna od absorpcije v prebavilih in od resnosti učinka "prvega prehoda" skozi jetra, zaradi česar neaktivni presnovki vstopijo v sistemski obtok (z izjemo beklometazonijevega 17-monopropionata, aktivnega presnovka beklometazondipropionata). Odmerki ICS do 1000 mcg / dan (za flutikazon do 500 mcg / dan) imajo rahel sistemski učinek.
Vsi ICS imajo hitro sistemsko razdaljo, primerljivo s količino jetrnega krvnega pretoka. To je eden od dejavnikov, ki zmanjšujejo sistemski učinek ICS.
Značilnosti najpogosteje uporabljenih zdravil
ICS vključuje beklometazon dipropionat, budezonid, flutikazon propionat, flunisolid, triamsinolon acetonid, mometazon furoat. Na voljo so v aerosolnih odmerkih, inhalatorjih v prahu in raztopinah za inhaliranje skozi razpršilec (budezonid).
Beklometazon dipropionat ... V klinični praksi se uporablja že več kot 20 let in ostaja eno najučinkovitejših in najpogosteje uporabljanih zdravil. Uporaba zdravila pri nosečnicah je dovoljena. Na voljo v obliki aerosolnega inhalatorja z odmerkom (Becotide 50 mcg, Becloforte 250 mcg, Aldecin 50 mcg, Beklokort 50 in 250 mcg, Beclomet 50 in 250 mcg / odmerek), inhalator z odmerkom, aktiviran z vdihavanjem (Beklazon Light Breathing 100 in 250 mcg / odmerek) , inhalator v prahu (Bekodisk 100 in 250 mcg / odmerek inhalator Diskhaler; večodmerni inhalator Easyhaler, Beclomet 200 mcg / odmerek). Za inhalatorja Bekotid in Becloforte so izdelani posebni distančniki - "Volumatic" (distančnik ventilov velikega volumna za odrasle) in "Babihaler" (distančnik 2 ventila majhne prostornine s silikonsko masko za obraz za majhne otroke).
Budezonid ... Sodobno zelo aktivno zdravilo. Uporablja se v obliki aerosolnega inhalatorja z odmerjenimi odmerki (Budesonide-Mite 50 mcg / odmerek; Budesonide-forte 200 mcg / odmerek), inhalatorja v prahu (Pulmicort Turbuhaler 200 mcg / odmerek; Benacort Cyclohaler 200 mcg / odmerek) in suspenzije za razpršilec 0,5 in 0,25 mg / odmerek). Pulmicort Turbuhaler je edina dozirna oblika ICS, ki ne vsebuje nosilca. Za inhalatorje z odmerjenimi odmerki Budesonide Mite in Budesonide Forte se izdela distančnik. Budezonid je sestavni del kombiniranega zdravila Symbicort.
Budezonid ima najugodnejši terapevtski indeks, kar je povezano z visoko afiniteto do glukokortikoidnih receptorjev in pospešeno presnovo po sistemski absorpciji v pljučih in črevesju. Budezonid je edini ICS, za katerega je bila dokazana možnost enkratne uporabe. Dejavnik, ki zagotavlja učinkovitost uporabe budezonida enkrat na dan, je zadrževanje budezonida v dihalih v obliki znotrajceličnega depoja zaradi reverzibilne esterifikacije (tvorba estrov maščobnih kislin). Z zmanjšanjem koncentracije prostega budezonida v celici se aktivirajo znotrajcelične lipaze, budezonid, ki se sprosti iz estrov, pa se ponovno veže na receptor. Podoben mehanizem ni značilen za druge kortikosteroide in omogoča podaljšanje protivnetnega učinka. Številne študije so pokazale, da je lahko znotrajcelično odlaganje pomembnejše glede aktivnosti zdravil kot afiniteta receptorjev.
Nedavne študije zdravila Pulmicort Turbuhaler so dokazale, da ne vpliva na končno rast pri dolgotrajni uporabi pri otrocih, mineralizaciji kosti, ne povzroča angiopatije in sive mrene. Pulmicort je priporočljiv tudi za uporabo pri nosečnicah: ugotovljeno je bilo, da njegova uporaba ne povzroča povečanja števila plodovih anomalij. Pulmicort Turbuhaler je prvi in \u200b\u200bedini ICS, ki ga je FDA (ameriška organizacija za nadzor nad drogami) uvrstila v kategorijo B na lestvici zdravil, predpisanih za nosečnost. Ta kategorija vključuje zdravila, ki jih je varno jemati med nosečnostjo. Preostali del ICS je kategoriziran kot "C" (jemanje med nosečnostjo ni priporočljivo).
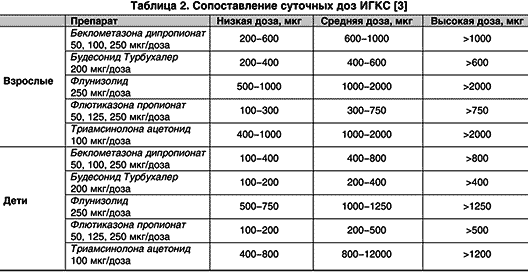
Flutikazon propionat ... Najbolj aktivno zdravilo doslej. Ima minimalno peroralno biološko uporabnost (<1%). Эквивалентные терапевтические дозы флютиказона почти в два раза меньше, чем у беклометазона и будесонида в аэрозольном ингаляторе и сопоставимы с дозами будесонида в Турбухалере (табл. 2). По данным ряда исследований, флютиказона пропионат больше угнетает надпочечники, но в эквивалентных дозах имеет сходную с другими ИГКС активность в отношении надпочечников.
Predstavlja se v obliki aerosolnega inhalatorja z odmerjenimi odmerki (Flixotide 50, 125 in 250 μg / odmerek) in inhalatorja v prahu (Flixotide Dischaler - rotadiski 50, 100, 250 in 500 μg / odmerek; Flixotide Multidisk 250 μg / odmerek). Za aerosolne inhalatorje se izdelujejo posebni distančniki - Volumatic (distančnik ventilov velikega volumna za odrasle) in Babihaler (distančnik 2 ventila majhne prostornine s silikonsko obrazno masko za majhne otroke). Flutikazon je sestavni del kombiniranega zdravila Seretide Multidisk.
Flunizolid ... Zdravilo z nizko glukokortikoidno aktivnostjo. Na domačem trgu ga predstavlja blagovna znamka Ingakort (inhalator z odmerkom 250 μg / odmerek z distančnikom). Kljub velikim terapevtskim odmerkom praktično nima sistemskih učinkov, ker se že ob prvem prehodu skozi jetra 95% pretvori v neaktivno snov. Trenutno se v klinični praksi redko uporablja.
Triamsinolon acetonid ... Zdravilo z nizko hormonsko aktivnostjo. Inhalator z odmerkom 100 mcg / odmerek. Blagovna znamka Azmakort, ki ni zastopana na ruskem trgu.
Mometazon furoat ... Zdravilo z visoko glukokortikoidno aktivnostjo. Na ruskem trgu je predstavljen samo v obliki pršila za nos Nazonex.
Klinična preskušanja, ki primerjajo učinkovitost ICS v obliki izboljšanja simptomov in kazalnikov dihalne funkcije, kažejo, da:
- Budezonid in beklometazon dipropionat v aerosolnih inhalatorjih pri enakih odmerkih se praktično ne razlikujeta po učinkovitosti.
- Flutikazon propionat zagotavlja enak učinek kot dvojni odmerki beklometazona ali budezonida v aerosolnih odmerkih.
- Budezonid, ki se daje preko Turbuhalerja, ima enak učinek kot dvojni budezonid v aerosolnem odmerku.
Neželeni učinki
Sodobni ICS so razvrščeni kot zdravila z visokim terapevtskim indeksom in imajo visok varnostni profil tudi pri dolgotrajni uporabi. Dodelite sistemske in lokalne neželene učinke. Sistemski neželeni učinki lahko postanejo klinično pomembni le, če se uporabljajo visoki odmerki. Odvisni so od afinitete zdravil do receptorja, lipofilnosti, obsega porazdelitve, razpolovne dobe, biološke uporabnosti in drugih dejavnikov. Tveganje sistemskih neželenih dogodkov za vse trenutno razpoložljive ICS je povezano z zaželenimi učinki na dihalne poti. Uporaba ICS v srednjih terapevtskih odmerkih zmanjšuje tveganje za sistemske učinke.
V bistvu so neželeni učinki ICS povezani z njihovo uporabo in se zmanjšajo na ustno kandidozo, hripavost, draženje sluznice in kašelj. Da bi se izognili tem pojavom, sta potrebna pravilna tehnika vdihavanja in individualna izbira ICS.
Kombinirana zdravila
Kljub dejstvu, da so ICS osnova terapije AD, ne omogočajo vedno popolnega nadzora nad vnetnim procesom v bronhialnem drevesu in s tem manifestacijami AD. V zvezi s tem je bilo treba na zahtevo ali redno predpisovati kratko delujoče β 2 -agoniste. Tako je nujno potreben nov razred zdravil, ki nimajo pomanjkljivosti, značilnih za kratko delujoče β 2-agoniste, in imajo dokazano dolgoročen zaščitni in protivnetni učinek na dihala.
Ustvarjeni so in se danes pogosto uporabljajo b 2 -agonisti, ki jih na farmacevtskem trgu zastopata dve zdravili: formoterol fumarat in salmeterol ksinafoat. V sodobnih smernicah za zdravljenje astme je v primeru nezadostnega nadzora BA z monoterapijo z inhalacijskim GCS (od druge faze) priporočljivo dodajanje dolgo delujočih β 2 -agonistov. Številne študije so pokazale, da je kombinacija inhalacijskih kortikosteroidov z dolgo delujočim b 2 -agonistom učinkovitejša od podvojitve odmerka inhalacijskih kortikosteroidov in vodi do pomembnejšega izboljšanja pljučne funkcije in boljšega nadzora simptomov astme. Izkazalo se je tudi, da zmanjšuje število poslabšanj in znatno izboljša kakovost življenja pri bolnikih, ki prejemajo kombinirano zdravljenje. Tako je pojav kombiniranih pripravkov, ki vsebujejo inhalacijski GCS in dolgo delujoči β 2 -agonist, odraz evolucije stališč o terapiji BA.
Glavna prednost kombiniranega zdravljenja je večja učinkovitost zdravljenja pri uporabi nižjih odmerkov ICS. Poleg tega kombinacija obeh zdravil v enem inhalatorju olajša pacientu upoštevanje zdravnikovih navodil in potencialno izboljša skladnost.
Seretid Multidisk ... Sestavni deli sta salmeterol ksinafoat in flutikazon propionat. Zagotavlja visoko raven nadzora nad simptomi astme. Uporablja se le kot osnovna terapija, predpiše se lahko že od druge faze. Zdravilo je predstavljeno v različnih odmerkih: 50/100, 50/250, 50/500 mcg salmeterol / flutikazon v 1 odmerku. Multidisk spada med inhalacijske naprave z nizko odpornostjo, kar omogoča uporabo pri bolnikih z zmanjšano stopnjo vdihavanja.
Symbicort Turbuhaler ... Sestavni deli so budezonid in formoterol fumarat. Na ruskem trgu je predstavljen v odmerku 160 / 4,5 mcg v 1 odmerku (odmerki zdravil so navedeni kot izhodni odmerek). Pomembna lastnost zdravila Symbicort je sposobnost uporabe tako za osnovno terapijo (za nadzor vnetnega procesa) kot za takojšnje lajšanje simptomov astme. To je predvsem posledica lastnosti formoterola (hiter začetek delovanja) in sposobnosti budezonida, da v 24 urah aktivno deluje na sluznico bronhialnega drevesa.
Symbicort omogoča individualno prilagodljivo odmerjanje (1-4 inhalacijski odmerki na dan). Zdravilo Symbicort se lahko uporablja od 2. stopnje, še posebej pa je indicirano za bolnike z nestabilno astmo, za katere so značilni nenadni hudi napadi težav z dihanjem.
Sistemski GCS Sistemski kortikosteroidi se uporabljajo predvsem za lajšanje poslabšanja astme. Peroralni kortikosteroidi so najučinkovitejši. Intravenski kortikosteroidi so predpisani za poslabšanje astme, če je bolj zaželen intravenski dostop ali v primeru motene absorpcije iz prebavil z uporabo velikih odmerkov (do 1 g prednizolona, \u200b\u200bmetilprednizolona in hidrokortizona). Kortikosteroidi povzročijo klinično pomembno izboljšanje 4 ure po njihovi uporabi.
Z poslabšanjem astme je prikazan kratek peroralni kortikosteroidi (7–14 dni), ki se začnejo z velikimi odmerki (30–60 mg prednizolona). V nedavnih publikacijah je za neživljenjsko nevarna poslabšanja priporočljiv naslednji kratek potek sistemskih kortikosteroidov: 6 tablet prednizolona zjutraj (30 mg) 10 dni, čemur sledi prekinitev zdravljenja. Čeprav so sheme zdravljenja sistemskih kortikosteroidov lahko drugačne, so temeljna načela njihovo imenovanje v velikih odmerkih za hiter učinek in posledično hitro umik. Ne smemo pozabiti, da mu je treba bolnika takoj, ko je pripravljen vzeti inhalacijske kortikosteroide, dodeliti postopoma.
Sistemske glukokortikoide je treba predpisati, če:
- Poslabšanje zmerno ali hudo.
- Uporaba kratko delujočih inhalacijskih β 2-agonistov na začetku zdravljenja ni privedla do izboljšanja.
- Poslabšanje se je razvilo kljub temu, da je bil bolnik dolgotrajno zdravljen s peroralnimi kortikosteroidi.
- Za nadzor predhodnih poslabšanj so bili potrebni peroralni kortikosteroidi.
- Trikrat ali večkrat na leto so bili izvedeni tečaji glukokortikoidov.
- Pacient je na mehaničnem prezračevanju.
- Prej so bila življenjsko nevarna poslabšanja.
Uporaba podaljšanih oblik sistemskih steroidov za lajšanje poslabšanj in vzdrževalno zdravljenje astme je nezaželena.
Za dolgotrajno zdravljenje hudih BA je treba predpisati sistemske kortikosteroide (metilprednizolon, prednizolon, triamsinolon, betametazon) v najmanjšem učinkovitem odmerku. Pri dolgotrajnem zdravljenju najmanj neželenih učinkov povzroči izmenično predpisovanje in dajanje zdravila v prvi polovici dneva (da se zmanjša učinek na cirkadijske ritme izločanja kortizola). Poudariti je treba, da je treba v vseh primerih predpisovanja sistemskih steroidov bolniku predpisati visoke odmerke kortikosteroidov za inhaliranje. Od peroralnih kortikosteroidov imajo prednost tisti z minimalno mineralokortikoidno aktivnostjo, razmeroma kratkim razpolovnim časom in omejenim učinkom na progaste mišice (prednizolon, metilprednizolon).
Zasvojenost s steroidi
Posebno pozornost je treba nameniti bolnikom, ki so prisiljeni nenehno jemati sistemske kortikosteroide. Obstaja več možnosti za nastanek odvisnosti od steroidov pri bolnikih z astmo in drugimi boleznimi, ki jih spremlja bronhialna obstrukcija:
- Pomanjkanje skladnosti (interakcije) med zdravnikom in pacientom.
- Neimenovanje inhalacijskega GCS bolnikom. Mnogi zdravniki menijo, da bolnikom, ki prejemajo sistemske steroide, ni treba predpisovati inhalacijskega GCS. Če bolnik z astmo prejme sistemske steroide, ga je treba obravnavati kot bolnika s hudo obliko astme z neposrednimi indikacijami za predpisovanje visokih odmerkov inhalacijskih kortikosteroidov.
- Pri bolnikih s sistemskimi boleznimi (vključno s pljučnim vaskulitisom, na primer Churg-Straussovim sindromom) lahko bronhialno obstrukcijo štejemo za AD. Umik sistemskih steroidov pri teh bolnikih lahko spremljajo hudi znaki sistemske bolezni.
- V 5% primerov se pojavi odpornost na steroide, za katero je značilna odpornost steroidnih receptorjev na steroidna zdravila. Trenutno ločimo dve podskupini: bolnike z resnično odpornostjo na steroide (tip II), ki pri dolgotrajnem dajanju visokih odmerkov sistemskega GCS nimajo stranskih učinkov, in bolnike s pridobljeno odpornostjo (tip I), ki imajo neželene učinke sistemskega GCS. V zadnji podskupini je odpornost mogoče premagati najverjetneje s povečanjem odmerka GCS in predpisovanjem zdravil z dodatnim učinkom.
1. Bronhialna astma. Globalna strategija: skupno poročilo Nacionalnega inštituta za srce, pljuča, kri in Svetovne zdravstvene organizacije. Pulmologija, 1996.
2. Bronhialna astma. Priročnik za zdravnike v Rusiji (sistem formul). "Pulmologija", dodatek-99.
3. Vodilna navodila pri diagnostiki in zdravljenju bronhialne astme. Povzetek poročila strokovne skupine EPR-2. Nacionalni inštitut za zdravje. Nacionalni inštitut za srce, pljuča in kri. Publikacija NIH-97. Prevod izd. Prof. Tsoi A. N., M, Grant, 1998.
4. Ilyina N.I. Inhalirani glukokortikoidi. Asthma.ru. Alergijske bolezni in bolezni dihal. 0 * 2001 (pilot).
5. Ogorodova L.M. Sistemi za inhalacijsko dovajanje zdravil v dihala. Pulmologija, 1999; Št. 1, 84-87
6. Formularni sistem: zdravljenje bronhialne astme. Astma. ru, 0. 2001, 6-9
7. Chuchalin A.G. Bronhialna astma. Moskva, 1997.
8. Tsoi A.N. Inhalirani glukokortikoidi: učinkovitost in varnost. RMJ 2001; 9: 182-185
9. Tsoi A.N. Primerjalna farmakokinetika inhalacijskih glukokortikoidov. Alergologija 1999; 3: 25-33
10. Agertoft L., Pedersen S. Učinek dolgotrajnega zdravljenja z inhaliranim budezonidom na odraslo višino pri otrocih z astmo. N Engl J Med 2000; 343: 1064-9
11. Ankerst J., Persson G., Weibull E. Bolniki z astmo so velik odmerek budezonida / formoterola v enem inhalatorju dobro prenašali. Eur Respir J 2000; 16 (Suppl 31): 33s + plakat
12. Barnes P.J. Inhalirani glukokortikoidi za astmo. N. Engl. Med. 1995; 332: 868-75
13. Beklometazon dipropionat in budezonid. Pregledani klinični dokazi. Respir Med 1998; 92 (priloga B)
14. Britanske smernice o obvladovanju astme. Thorax, 1997; 52 (priloga 1) 1–20.
15. Burney PGJ. Aktualna vprašanja v epidemiologiji astme, v Holgate ST, et al, Asthma: Physiology. Imunologija in zdravljenje. London, Academic Press, 1993, str. 3-25.
16. Crisholm S et al. Budezonid enkrat na dan pri blagi astmi. Respir Med 1998; 421-5
17. Kips JC, O / Connor BJ, Inman MD, Svensson K, Pauwels RA, O / Byrne PM. Dolgoročna študija protivnetnega učinka nizko odmerjenega budezonida in formoterola v primerjavi z visoko odmerjenim budezonidom pri astmi. Am Respir Crit Care Med 2000; 161: 996-1001
18. McFadden ER, Casale TB, Edwards TB et al. Dajanje budezonida enkrat na dan s pomočjo zdravila Turbuhaler osebam s stabilno astmo. J Allergy Clin Immunol 1999; 104: 46-52
19. Miller-Larsson A., Mattsson H., Hjertberg E., Dahlback M., Tunek A., Brattsand R. Reverzibilna konjugacija maščobnih kislin budezonida: nov mehanizem, ki podaljša zadrževanje lokalno apliciranega steroida v tkivu dihalnih poti. Drug Metab Dispos 1998; 26: 623-30
20. Miller-Larsson A. et al. Dolgotrajna aktivnost dihalnih poti in izboljšana selektivnost budezonida, verjetno zaradi esterifikacije. Am J Respir Crit Care Med 2000; 162: 1455-1461
21. Pauwels RA et al. Vpliv inhalacijskega formoterola in budezonida na poslabšanje astme. N Engl J Med 1997; 337: 1405-11
22. Pedersen S, O / Byrne P. Primerjava učinkovitosti in varnosti inhalacijskih kortikosteroidov pri astmi. Alergija 1997; 52 (priloga 39): 1-34.
23. Woolcock A. et al. Primerjava dodajanja salmeterola inhalacijskim steroidom s podvojitvijo odmerka inhalacijskih steroidov. Am J Respir Crit Care Med 1996,153,1481-8.
Hvala vam
Spletno mesto vsebuje osnovne informacije samo v informativne namene. Diagnozo in zdravljenje bolezni je treba izvajati pod nadzorom strokovnjaka. Vsa zdravila imajo kontraindikacije. Potreben je strokovni posvet!
Uvod (značilnosti zdravil)
Naravni kortikosteroidi
 Kortikosteroidi - pogosto ime hormoni nadledvične skorje, ki vključujejo glukokortikoide in mineralokortikoide. Glavna glukokortikoida, ki nastaneta v človeški skorji nadledvične žleze, sta kortizon in hidrokortizon, mineralokortikoid pa aldosteron.
Kortikosteroidi - pogosto ime hormoni nadledvične skorje, ki vključujejo glukokortikoide in mineralokortikoide. Glavna glukokortikoida, ki nastaneta v človeški skorji nadledvične žleze, sta kortizon in hidrokortizon, mineralokortikoid pa aldosteron. Kortikosteroidi imajo v telesu veliko zelo pomembnih funkcij.
Glukokortikoidi nanašati se na steroidiz protivnetnim delovanjem sodelujejo pri uravnavanju presnove ogljikovih hidratov, maščob in beljakovin, nadzorujejo puberteto, delovanje ledvic, odziv telesa na stres in prispevajo k normalnemu poteku nosečnosti. Kortikosteroidi se inaktivirajo v jetrih in izločijo z urinom.
Aldosteron uravnava presnovo natrija in kalija. Tako pod vplivom mineralokortikoidi Na + se zadrži v telesu in izločanje ionov K + iz telesa se poveča.
Sintetični kortikosteroidi
Sintetični kortikosteroidi z enakimi lastnostmi kot naravni so našli praktično uporabo v medicinski praksi. Sposobni so začasno zatreti vnetni proces, vendar ne vplivajo na nalezljiv izvor in povzročitelje bolezni. Ko zdravilo kortikosteroid preneha delovati, se okužba nadaljuje.Kortikosteroidi povzročajo napetost in stres v telesu, kar vodi do zmanjšanja imunosti, saj je imunost zagotovljena na zadostni ravni le v sproščenem stanju. Glede na zgoraj navedeno lahko rečemo, da uporaba kortikosteroidov prispeva k daljšemu poteku bolezni, blokira proces regeneracije.
Poleg tega sintetični kortikosteroidi zavirajo delovanje naravnih hormonskih kortikosteroidov, kar vodi v okvaro nadledvične funkcije na splošno. Kortikosteroidi vplivajo tudi na delo drugih žlez z notranjim izločanjem, poruši se hormonsko ravnovesje telesa.
Kortikosteroidna zdravila z odstranjevanjem vnetja delujejo tudi analgetično. Med sintetična kortikosteroidna zdravila spadajo deksametazon, prednizolon, Sinalar, triamcinolon in drugi. Ta zdravila so bolj aktivna in povzročajo manj neželenih učinkov kot naravna.
Oblike sproščanja kortikosteroidov
Kortikosteroidi so na voljo v obliki tablet, kapsul, raztopin v ampulah, mazil, linimenta, krem. (Prednizolon, Deksametazon, Budenofalm, Kortizon, Cortinef, Medrol).Notranji pripravki (tablete in kapsule)
- Prednizolon;
- Celeston;
- Triamcinolon;
- Kenacort;
- Kortineff;
- Polkortolon;
- Kenalog;
- Metipred;
- Ječmenov vrt;
- Florinef;
- Medrol;
- Lemod;
- Decadron;
- Urbazon in drugi.
Priprave za injiciranje
- Prednizolon;
- Hidrokortizon;
- Diprospan (betametazon);
- Kenalog;
- Flosteron;
- Medrol in sod.
Lokalni pripravki (aktualni)
- Prednizolon (mazilo);
- Hidrokortizon (mazilo);
- Lokoid (mazilo);
- Corteid (mazilo);
- Afloderm (smetana);
- Latikort (smetana);
- Dermovate (krema);
- Fluorocort (mazilo);
- Lorinden (mazilo, losjon);
- Sinaflan (mazilo);
- Flucinar (mazilo, gel);
- Clobetasol (mazilo) itd.
Šibko aktivna sredstva: Prednizolon, hidrokortizon, Corteid, Locoid;
Zmerno aktiven: Afloderm, Latikort, Dermovate, Ftorokort, Lorinden;
Zelo aktiven: Akriderm, Advantan, Kuterid, Apulein, Kutiveyt, Sinaflan, Sinalar, Sinoderm, Flucinar.
Zelo zelo aktiven: Clobetasol.
Vdihani kortikosteroidi

- Beklametazon v obliki aerosolnih odmerkov (Bekotid, Aldecim, Beclomet, Beklokort); v obliki bekodiskov (prašek v enem odmerku, vdihnjen z dischalerjem); v obliki odmerjenega aerosola za vdihavanje skozi nos (beklometazon-nazalni, Beconase, Aldecim);
- Flunizolid v obliki odmerjenih aerosolov z distančnikom (Ingacort) za nazalno uporabo (Sintaris);
- Budezonid - doziran aerosol (Pulmicort), za nosno uporabo - Rinocort;
- Flutikazon v obliki aerosolov Flixotide in Fliksonase;
- Triamcinolon - aerosol z odmerkom z distančnikom (Azmakort), za nosno uporabo - Nazacort.
Indikacije za uporabo
Kortikosteroidi se uporabljajo za zatiranje vnetnega procesa v mnogih vejah medicine pri številnih boleznih.Indikacije za uporabo glukokortikoidov
- Revmatizem;
- revmatoidni in druge vrste artritisa;
- kolagenoze, avtoimunske bolezni (skleroderma, sistemski eritematozni lupus, periarteritis nodosa, dermatomiozitis);
- bolezni krvi (mieloblastna in limfoblastna levkemija);
- nekatere vrste malignih novotvorb;
- kožne bolezni (nevrodermatitis, luskavica, ekcem, seboroični dermatitis, diskoidni eritematozni lupus, atopijski dermatitis, eritroderma, lišaj planus);
- bronhialna astma;
- alergijske bolezni;
- pljučnica in bronhitis, fibrozni alveolitis;
- ulcerozni kolitis in Crohnova bolezen;
- akutni pankreatitis;
- hemolitična anemija;
- virusne bolezni (nalezljiva mononukleoza, virusni hepatitis in drugi);
- zunanji otitis (akutni in kronični);
- zdravljenje in preprečevanje šoka;
- v oftalmologiji (za neinfekcijske bolezni: iritis, keratitis, iridociklitis, skleritis, uveitis);
- nevrološke bolezni (multipla skleroza, akutna poškodba hrbtenjače, optični nevritis;
- s presaditvijo organov (za zatiranje zavrnitve).
Indikacije za uporabo mineralokortikoidov
- Addisonova bolezen (kronična insuficienca hormonov nadledvične skorje);
- miastenija gravis (avtoimunska bolezen, ki se kaže v mišični oslabelosti);
- motnje presnove mineralov;
- šibkost in mišična oslabelost.
Kontraindikacije
 Kontraindikacije za imenovanje glukokortikoidov:
Kontraindikacije za imenovanje glukokortikoidov:- preobčutljivost za zdravilo;
- hude okužbe (razen tuberkuloznega meningitisa in septičnega šoka);
- imunizacija z živim cepivom.
Kontraindikacije za imenovanje mineralokortikoidov:
- visok krvni pritisk;
- diabetes;
- nizka raven kalija v krvi;
- odpoved ledvic in jeter.
Neželeni učinki in previdnostni ukrepi
Kortikosteroidi lahko povzročijo najrazličnejše neželene učinke. Pri uporabi šibkih ali zmerno aktivnih učinkov so neželeni učinki manj izraziti in se redko pojavijo. Veliki odmerki zdravil in uporaba visoko aktivnih kortikosteroidov lahko pri dolgotrajni uporabi povzročijo naslednje neželene učinke:- pojav edema zaradi zadrževanja natrija in vode v telesu;
- zvišan krvni tlak;
- zvišan krvni sladkor (morda celo razvoj steroidnega diabetesa mellitusa);
- osteoporoza zaradi povečanega izločanja kalcija;
- aseptična nekroza kostnega tkiva;
- poslabšanje ali pojav razjede želodca; krvavitev iz prebavil;
- povečana tvorba trombov;
- povečanje telesne teže;
- pojav bakterijskih in glivičnih okužb zaradi zmanjšanja imunosti (sekundarna imunska pomanjkljivost);
- kršitev menstrualnega ciklusa;
- nevrološke motnje;
- razvoj glavkoma in sive mrene;
- atrofija kože;
- povečano potenje;
- pojav aken;
- zatiranje procesa regeneracije tkiva (počasno celjenje ran);
- odvečna rast dlak na obrazu;
- zatiranje delovanja nadledvične žleze;
- nestabilnost razpoloženja, depresija.
- prekomerno odlaganje maščobe na določenih delih telesa: na obrazu (tako imenovani "lunin obraz"), na vratu ("bikov vrat"), prsnem košu, na trebuhu;
- mišice udov so atrofirane;
- modrice na koži in strije (strije) na trebuhu.
Da bi zmanjšali tveganje za nastanek neželenih učinkov, je pomembno, da se pravočasno odzovemo na njihov videz, prilagodimo odmerke (če je le mogoče majhne odmerke), nadzorujemo telesno težo in vsebnost kalorij v zaužitih živilih ter omejimo uporabo natrijevega klorida in tekočine.
Kako uporabljati kortikosteroide?
 Glukokortikosteroidi se lahko uporabljajo sistemsko (v obliki tablet in injekcij), lokalno (intraartikularno, rektalno), lokalno (mazila, kapljice, aerosoli, kreme).
Glukokortikosteroidi se lahko uporabljajo sistemsko (v obliki tablet in injekcij), lokalno (intraartikularno, rektalno), lokalno (mazila, kapljice, aerosoli, kreme). Režim odmerjanja predpiše zdravnik. Pripravek tablet je treba jemati od 6. ure zjutraj (prvi odmerek) in najpozneje do 14. ure pozneje. Takšni pogoji sprejema so potrebni za približevanje fiziološkega pretoka glukokortikoidov v kri med njihovo proizvodnjo v nadledvični skorji.
V nekaterih primerih zdravnik odmerek pri velikih odmerkih in glede na naravo bolezni porazdeli za enakomeren vnos čez dan za 3-4 odmerke.
Tablete je treba jemati ob obroku ali takoj po obroku z malo vode.
Zdravljenje s kortikosteroidi
Obstajajo takšne vrste terapije s kortikosteroidi:- intenzivno;
- omejujoča;
- izmenično;
- občasno;
- pulzna terapija.
Omejujoča terapija uporablja se za dolgotrajne kronične procese - tablete se praviloma uporabljajo več mesecev ali celo let.
Za zmanjšanje zaviralnega učinka na delovanje žlez z notranjim izločanjem se uporabljajo intermitentni režimi zdravil:
- izmenično zdravljenje - uporabljajte glukokortikoide s kratkim in srednjim trajanjem delovanja (prednizolon, metilprednizolon) enkrat od 6. do 8. ure zjutraj vsakih 48 ur;
- intermitentna terapija - kratki, 3-4-dnevni tečaji jemanja zdravila s 4-dnevnimi odmori med njimi;
- pulzna terapija - hitro intravensko dajanje velikega odmerka (vsaj 1 g) zdravila za nujno oskrbo. Izbrano zdravilo za to zdravljenje je metilprednizolon (lažje je na voljo za dajanje na prizadeto območje in ima manj neželenih učinkov).
- Nizka - manj kot 7,5 mg;
- Srednje - 7,5-30 mg;
- Visoko - 30-100 mg;
- Zelo visoko - nad 100 mg;
- Impulzna terapija - nad 250 mg.
Za preventivo Neželeni učinki kortikosteroidov na prebavila pred jemanjem tablet, lahko priporočite uporabo Almagel, žele. Priporočljivo je izključiti kajenje, zlorabo alkoholnih pijač; zmerna vadba.
Kortikosteroidi za otroke
Sistemski glukokortikoidi dodeljena otrokom izključno zaradi absolutnih indikacij. V primeru sindroma bronhialne obstrukcije, ki ogroža otrokovo življenje, se uporablja intravensko dajanje prednizolona v odmerku 2-4 mg na 1 kg otrokove telesne teže (odvisno od resnosti poteka bolezni), v odsotnosti učinka pa se odmerek poveča za 20-50% vsake 2-4 ure, dokler pridobivanje učinka. Po tem se zdravilo takoj prekliče, brez postopnega zmanjšanja odmerka.Otroci s hormonsko odvisnostjo (na primer z bronhialno astmo) po intravenski uporabi zdravila postopoma preidejo v vzdrževalni odmerek prednizolona. Pri pogostih recidivih astme se Beklametazon dipropionat uporablja v obliki inhalacij - odmerek se izbere individualno. Po prejemu učinka se odmerek postopoma zmanjša na vzdrževalni (izbere se individualno).
Lokalni glukokortikoidi (kreme, mazila, losjoni) se uporabljajo v otroški praksi, vendar imajo otroci večjo nagnjenost k sistemskemu delovanju zdravil kot odrasli bolniki (upočasnjen razvoj in rast, Itsenko-Cushingov sindrom, zaviranje delovanja žlez z notranjim izločanjem). To je zato, ker imajo otroci večje razmerje med telesno površino in težo kot odrasli.
Iz tega razloga je treba topikalne glukokortikoide pri otrocih uporabljati le na omejenih območjih in v kratkem tečaju. To še posebej velja za novorojenčke. Za otroke prvega leta življenja lahko uporabljate samo mazila, ki ne vsebujejo več kot 1% hidrokortizona, ali zdravilo četrte generacije - Prednicarbat (Dermatol), pri starosti 5 let pa hidrokortizon 17-butirat ali mazila z zdravili srednje moči.
Za zdravljenje otrok, starejših od 2 let, se lahko zdravilo Mometasone uporablja po navodilih zdravnika (mazilo s podaljšanim učinkom, ki se uporablja 1 p. Na dan).
Obstajajo tudi druga zdravila za zdravljenje atopijskega dermatitisa pri otrocih z manj izrazitim sistemskim učinkom, na primer Advantan. Uporablja se lahko do 4 tedne, vendar je njegova uporaba omejena zaradi možnosti lokalnih neželenih reakcij (suhost in redčenje kože). V vsakem primeru izbira zdravila za zdravljenje otroka ostane pri zdravniku.
Kortikosteroidi med nosečnostjo in dojenjem
 Uporaba glukokortikoidov, tudi kratkotrajna, lahko v prihodnjih desetletjih "programira" delo mnogih organov in sistemov pri nerojenem otroku (nadzor krvnega tlaka, presnovni procesi, oblikovanje vedenja). Sintetični hormon posnema materin signal stresa za plod in tako prisili plod, da prisili uporabo rezerv.
Uporaba glukokortikoidov, tudi kratkotrajna, lahko v prihodnjih desetletjih "programira" delo mnogih organov in sistemov pri nerojenem otroku (nadzor krvnega tlaka, presnovni procesi, oblikovanje vedenja). Sintetični hormon posnema materin signal stresa za plod in tako prisili plod, da prisili uporabo rezerv. Ta negativni učinek glukokortikoidov povečuje dejstvo, da sodobna dolgotrajna zdravila (Metipred, Dexametazon) s placentnimi encimi ne deaktivirajo in imajo dolgoročen učinek na plod. Glukokortikoidi z zatiranjem imunskega sistema pomagajo zmanjšati odpornost nosečnice na bakterijske in virusne okužbe, kar lahko negativno vpliva tudi na plod.
Glukokortikoidna zdravila lahko nosečnici predpišemo le, če rezultat njihove uporabe presega tveganje za možne negativne posledice za plod.
Takšne indikacije so lahko:
1.
Grožnja prezgodnjega poroda (kratek potek hormonov izboljša pripravljenost prezgodnjega ploda na porod); uporaba površinsko aktivne snovi za otroka po rojstvu je omogočila zmanjšanje uporabe hormonov pri tej indikaciji.
2.
Revmatizem in avtoimunske bolezni v aktivni fazi.
3.
Dedna (intrauterina) hiperplazija pri plodu nadledvične skorje je težko diagnosticirati bolezen.
Prej je obstajala praksa predpisovanja glukokortikoidov za vzdrževanje nosečnosti. Toda prepričljivi podatki o učinkovitosti takšne tehnike niso bili pridobljeni, zato se trenutno ne uporablja.
V porodniški praksi Pogosteje se uporabljajo metipred, prednizolon in deksametazon. V posteljico prodrejo na različne načine: prednizolon v večji meri uničijo encimi v posteljici, deksametazon in Metipred pa le za 50%. Če se torej hormonska zdravila uporabljajo za zdravljenje nosečnice, je bolje predpisati prednizolon, za zdravljenje ploda pa deksametazon ali Metipred. V zvezi s tem so prednizolon in neželeni učinki pri plodu manj pogosti.
Glukokortikoidi za hude alergije so predpisani tako sistemsko (injekcije ali tablete) kot lokalni (mazila, geli, kapljice, inhalacije). Imajo močan antialergijski učinek. V glavnem se uporabljajo naslednja zdravila: hidrokortizon, prednizolon, deksametazon, betametazon, beklometazon.
Od lokalnih glukokortikoidov (za lokalno zdravljenje) se v večini primerov uporabljajo intranazalni aerosoli: za seneni nahod, alergijski rinitis, zamašen nos (kihanje). Običajno imajo dober učinek. Široko se uporabljajo flutikazon, dipropionat, propionat in drugi.
Pri alergijskem konjunktivitisu se zaradi večjega tveganja neželenih učinkov glukokortikoidi redko uporabljajo. Vsekakor pa v primeru alergijskih manifestacij hormonskih zdravil ni mogoče uporabljati samostojno, da bi se izognili neželenim posledicam.
Kortikosteroidi za luskavico
 Glukokortikoide za luskavico je treba uporabljati predvsem v obliki mazil in krem. Sistemska (injekcije ali tablete) hormonska zdravila lahko prispevajo k hujši luskavici (pustularni ali pustulozni) in jih zato ne priporočamo.
Glukokortikoide za luskavico je treba uporabljati predvsem v obliki mazil in krem. Sistemska (injekcije ali tablete) hormonska zdravila lahko prispevajo k hujši luskavici (pustularni ali pustulozni) in jih zato ne priporočamo. Glukokortikoidi za lokalno uporabo (mazila, kreme) se običajno uporabljajo 2 str. na dan: kreme podnevi brez povojev in ponoči skupaj s premogovim katranom ali antralinom z okluzivnim povojem. Pri obsežnih lezijah se za zdravljenje celotnega telesa uporablja približno 30 g zdravila.
Izbira glukokortikoidnega zdravila glede na stopnjo aktivnosti za lokalno uporabo je odvisna od resnosti poteka luskavice in njene razširjenosti. Ker se lezije luskavice med zdravljenjem zmanjšujejo, je treba zdravilo spremeniti v manj aktivno (ali ga uporabljati redkeje), da se pojavijo neželeni učinki. Če pride do učinka po približno 3 tednih, je bolje, da hormonsko zdravilo 1-2 tedna zamenjate z mehčalcem.
Dolgotrajna uporaba glukokortikoidov na velikih površinah lahko poslabša postopek. Ponovitev luskavice po prekinitvi zdravljenja se zgodi prej kot pri zdravljenju brez uporabe glukokortikoidov.
, Coaxil, Imipramine in drugi) v kombinaciji z glukokortikoidi lahko povzročijo zvišanje očesnega tlaka.
Pravila za umik kortikosteroidov
Pri dolgotrajni uporabi glukokortikoidov mora biti odvajanje zdravila postopno. Glukokortikoidi zavirajo delovanje nadledvične skorje, zato se lahko s hitrim ali nenadnim umikom zdravila razvije nadledvična insuficienca. Ni standardiziranega režima odvzema kortikosteroidov. Način odpovedi in zmanjšanja odmerka je odvisen od trajanja predhodnega zdravljenja.Če trajanje glukokortikoida traja nekaj mesecev, lahko odmerek prednizolona zmanjšamo za 2,5 mg (0,5 tablete) vsakih 3-5 dni. Pri daljšem trajanju tečaja se odmerek zmanjša počasneje - za 2,5 mg na 1-3 tedne. Z veliko previdnostjo se odmerek zmanjša pod 10 mg - 0,25 tablete vsakih 3-5-7 dni.
Če je bil začetni odmerek prednizolona visok, je na začetku zmanjšanje intenzivnejše: za 5-10 mg vsake 3 dni. Ko dosežete dnevni odmerek, enak 1/3 začetnega odmerka, ga zmanjšajte za 1,25 mg (1/4 tablete) vsaka 2-3 tedna. Zaradi tega zmanjšanja bolnik prejme vzdrževalne odmerke eno leto ali več.
Režim zmanjševanja zdravil predpiše zdravnik, kršitev tega režima pa lahko povzroči poslabšanje bolezni - zdravljenje se bo moralo znova začeti z večjim odmerkom.
Cene kortikosteroidov
 Ker je na trgu toliko kortikosteroidov v različnih oblikah, je tukaj naštetih le nekaj:
Ker je na trgu toliko kortikosteroidov v različnih oblikah, je tukaj naštetih le nekaj: - Hidrokortizon - suspenzija - 1 steklenica 88 rubljev; mazilo za oči 3 g - 108 rubljev;
- Prednizolon - 100 tablet 5 mg - 96 rubljev;
- Metipred - 30 tablet po 4 mg - 194 rubljev;
- Metipred - 250 mg 1 steklenica - 397 rubljev;
- Triderm - mazilo 15 g - 613 rubljev;
- Triderm - smetana 15 g - 520 rubljev;
- Dexamed - 100 ampul po 2 ml (8 mg) - 1377 rubljev;
- Deksametazon - 50 tablet po 0,5 mg - 29 rubljev;
- Deksametazon - 10 ampul po 1 ml (4 mg) - 63 rubljev;
- Oftan Dexametazon - kapljice za oko 5 ml - 107 rubljev;
- Medrol - 50 tablet po 16 mg - 1.083 rubljev;
- Flixotide - aerosol 60 odmerkov - 603 rubljev;
- Pulmicort - aerosol 100 odmerkov - 942 rubljev;
- Benacort - aerosol 200 odmerkov - 393 rubljev;
- Symbicort - aerosol z razpršilnikom 60 odmerkov - 1313 rubljev;
- Beklazon - aerosol 200 odmerkov - 475 rubljev.
Glukokortikosteroidi kot glavna zdravila za zdravljenje astme. ICS.
Kot veste, je v središču poteka bronhialne astmemi (BA) je kronično vnetje in glavno zdravljenje te bolezni jeuporaba protivnetnih zdravil. Danes so glukokortikosteroidi prepoznaniglavna zdravila za zdravljenje astme.
Sistemski kortikosteroidi so še vedno izbrana zdravila pri zdravljenju poslabšanja astme, vendar se je konec 60. let prejšnjega stoletja začelo novo obdobje zdravljenja astme in je bilo povezano z nastankom in uvedbo inhalacijskih glukokortikosteroidov (ICS) v klinično prakso.
ICS pri zdravljenju bolnikov z astmo trenutno veljajo za zdravila prve izbire. Glavna prednost ICS je neposredna dostava aktivne snovi v dihala in ustvarjanje tam višjih koncentracij zdravila, hkrati pa odpravlja ali zmanjšuje sistemske neželene učinke. Za prvo zdravljenje z astmo so bili ustvarjeni aerosoli vodotopnega hidrokortizona in prednizolona. Vendar pa je bila njihova uporaba zaradi visokega sistemskega in nizkega protivnetnega učinka neučinkovita. V začetku sedemdesetih let. lipofilni glukokortikosteroidi so bili sintetizirani z visokim lokalnim protivnetnim delovanjem in šibkim sistemskim delovanjem. Tako so ICS trenutno postala najučinkovitejša zdravila za osnovno terapijo astme pri pacientih katere koli starosti (stopnja dokaza A).
ICS lahko zmanjša resnost simptomov astme, zavira aktivnost alergijskega vnetja, zmanjša hiperreaktivnost bronhijev na alergene in nespecifične dražilne snovi (gibanje, hladen zrak, onesnaževala itd.), Izboljša prepustnost bronhijev, izboljša kakovost življenja pacientov in zmanjša število odsotnosti z dela zaradi šolanja in dela. Dokazano je, da uporaba ICS pri bolnikih z astmo vodi do znatnega zmanjšanja števila poslabšanj in hospitalizacij, zmanjšuje umrljivost zaradi astme in preprečuje tudi razvoj nepopravljivih sprememb v dihalnih poteh (raven dokazov A). ICS se uspešno uporablja tudi za zdravljenje KOPB in alergijskega rinitisa kot najmočnejša protivnetna zdravila.
V nasprotju s sistemskimi glukokortikosteroidi je za ICS značilna velika afiniteta do receptorjev, nižji terapevtski odmerki in minimalno število neželenih učinkov.
Premoč ICS pri zdravljenju astme nad drugimi skupinami protivnetnih zdravil ni dvoma in danes so po mnenju večine domačih in tujih strokovnjakov ICS najučinkovitejša zdravila za zdravljenje bolnikov z astmo. Toda tudi na dobro preučenih področjih medicine obstajajo premalo utemeljene in včasih napačne ideje. Do danes potekajo razprave o tem, kako zgodaj je treba začeti zdravljenje z ICS, v kakšnih odmerkih, kakšnem ICS in s katero dostavno napravo, kako dolgo izvajati terapijo, in kar je najpomembneje, kako zagotoviti, da predpisana terapija z ICS ne škoduje telesu. tiste. sistemski učinki in drugi neželeni učinki kortikosteroidov se ne kažejo. Z dokazi podprta medicina je usmerjena v boj proti takim težnjam, ki so po mnenju zdravnikov in bolnikov zmanjšale učinkovitost zdravljenja in preprečevanja astme.
V klinični praksi se trenutno uporabljajo naslednji ICS: beklometazon dipropionat (BDP), budezonid (BUD), flutikazon propionat (FP), triamcinolon acetonid (TAA), flunisolid (FLU) in mometazon furoat (MF). Učinkovitost terapije z ICS je neposredno odvisna od: zdravilne učinkovine, odmerka, oblike in načina dajanja, skladnosti. čas začetka zdravljenja, trajanje terapije, resnost poteka (poslabšanje) astme in KOPB.
Kateri ICS je bolj učinkovit?
Pri enakovrednih odmerkih so vsi ICS enako učinkoviti (dokaz A). Farmakokinetiko zdravil in s tem terapevtsko učinkovitost določajo fizikalno-kemijske lastnosti molekul GCS. Ker je molekularna struktura ICS različna, imajo različno farmakokinetiko in farmakodinamiko. Za primerjavo klinične učinkovitosti in možnih neželenih učinkov ICS se predlaga uporaba terapevtskega indeksa, razmerja pozitivnih (zaželenih) kliničnih in neželenih (neželenih) učinkov, z drugimi besedami, učinkovitost ICS ocenjujejo glede na njihovo sistemsko delovanje in lokalno protivnetno aktivnost. Z visokim terapevtskim indeksom je boljše razmerje učinek / tveganje. Številni farmakokinetični parametri so pomembni za določanje terapevtskega indeksa. Tako protivnetno (lokalno) aktivnost ICS določajo naslednje lastnosti zdravil: lipofilnost, ki jim omogoča hitrejši in boljši zajem iz dihalnih poti in daljše zadrževanje v tkivih dihal; afiniteta do receptorjev GCS; visok primarni učinek inaktivacije v jetrih; trajanje komunikacije s ciljnimi celicami.
Eden najpomembnejših kazalnikov je lipofilnost, ki je povezana z afiniteto zdravila za steroidne receptorje in razpolovno dobo. Višja kot je lipofilnost, učinkovitejše je zdravilo, saj zlahka prodre skozi celične membrane in poveča kopičenje v pljučnem tkivu. To poveča trajanje njegovega delovanja na splošno in lokalni protivnetni učinek z oblikovanjem rezervoarja zdravila.
Lipofilnost je najbolj izrazita pri AF, sledita ji BDP in BUD pri tem kazalniku. ... FP in MF sta zelo lipofilni spojini, zato imata večji obseg porazdelitve v primerjavi z zdravili, ki so manj lipofilna, BUD, TAA. BUD je približno 6-8-krat manj lipofilna kot AF in zato 40-krat manj lipofilna kot BDP. Številne študije so hkrati pokazale, da se v pljučnem tkivu zadrži manj lipofilnega BUD dlje kot AF in BDP. To je posledica lipofilnosti konjugatov budezonida z maščobnimi kislinami, ki je desetkrat večja od lipofilnosti nepoškodovanega BUD, ki zagotavlja trajanje njegovega bivanja v tkivih dihal. Znotrajcelična zaestritev BUD z maščobnimi kislinami v tkivih dihal vodi do lokalnega zadrževanja in nastanka "depoja" neaktivnega, a počasi obnavljajočega se prostega BUD. Poleg tega lahko velika znotrajcelična rezerva konjugiranega BUD in postopno sproščanje prostega BUD iz konjugirane oblike podaljša nasičenost receptorja in protivnetno aktivnost BUD, kljub manjši afiniteti do GCS receptorja v primerjavi s FP in BDP.
AF ima največjo afiniteto do receptorjev za GCS (približno 20-krat večjo kot aksidin deksametazona, 1,5-krat višjo od afinitete aktivnega presnovka BDP-17-BMP in 2-krat višjo od afinitete BUD). Indeks afinitete za receptorje BUD je 235, BDP - 53, FP - 1800. A kljub dejstvu, da je indeks afinitete BDP najnižji, je zelo učinkovit zaradi pretvorbe v monopropionat, ki ima ob zaužitju indeks afinitete 1400. To je najbolj aktiven po afiniteti za receptorje GCS sta FP in BDP.
Kot veste, se učinkovitost zdravila ocenjuje glede na njegovo biološko uporabnost. Biološka uporabnost ICS je sestavljena iz biološke uporabnosti odmerka, absorbiranega iz prebavil, in biološke uporabnosti odmerka, absorbiranega iz pljuč.
Visok odstotek odlaganja zdravil v intrapulmonalnih dihalnih poteh običajno daje najboljši terapevtski indeks za tiste ICS, ki imajo nizko sistemsko biološko uporabnost zaradi absorpcije iz sluznice ustne votline in prebavil. To na primer velja za BDP, ki ima sistemsko biološko uporabnost zaradi črevesne absorpcije, v nasprotju z BUD, ki ima sistemsko biološko uporabnost predvsem zaradi pljučne absorpcije. Pri ICS z nično biološko uporabnostjo (FP) je učinkovitost zdravljenja odvisna samo od vrste naprave za dajanje zdravila in tehnike vdihavanja, ti parametri pa ne vplivajo na terapevtski indeks.
Kar zadeva presnovo ICS, se BDP v 10 minutah hitro presnovi v jetrih, pri čemer nastane en aktivni presnovek - 17BMP in dva neaktivna - beklometazon 21- monopropionat (21-BMN) in beklometazon. FPv jetrih se hitro in popolnoma inaktivira s tvorbo enega delno aktivnega (1% aktivnosti EP) presnovka - 17β-karboksilne kisline. Budezonid se hitro in v celoti presnovi v jetrih s sodelovanjem citokroma p450 3A (CYP3A) z nastankom dveh glavnih presnovkov:6β-hidroksibudezonid (tvori oba izomera) in16β-hidroksiprednizolon (tvori samo 22R). Oba presnovka imata šibko farmakološko vrednostdejavnosti.
Primerjava uporabljenih ICS je težka zaradi razlik v njihovi farmakokinetiki in farmakodinamiki. V vseh preučevanih parametrih farmakokinetike in farmakodinamike je AF boljši od drugih ICS. Nedavne študije kažejo, da je AF v enakih odmerkih vsaj dvakrat bolj učinkovit kot BDP in BUD.
Pred kratkim objavljeni rezultati metaanalize 14 primerjalnih kliničnih študij: AF z BDP (7 študij) ali EUD (7 študij). V vseh 14 študijah so AF predpisali v polovičnem (ali manj) odmerku v primerjavi z BDP ali BUD. Pri primerjavi učinkovitosti BDP (400/1600 μg / dan) z AF (200/800 μg / dan) avtorji v nobeni od 7 analiziranih študij niso našli pomembnih razlik v dinamiki jutranjega največjega volumetričnega izdihavalnega pretoka (PEFR). Klinična učinkovitost in koncentracija kortizola v serumu se zjutraj niso bistveno razlikovali. Pri primerjavi učinkovitosti FUD (400/1600 μg / dan) in AF (200/800 μg / dan) je bilo dokazano, da AF bistveno bolj poveča PEFR kot učinek FUD. Pri uporabi majhnih odmerkov zdravil med njimi ni razlike v smislu zniževanja ravni kortizola v serumu zjutraj, vendar je bilo pri uporabi večjih odmerkov zdravil ugotovljeno, da AF vpliva na ta kazalnik v manjši meri. Tako rezultati metaanalize kažejo, da je učinkovitost BDP in AF pri polovičnem odmerku enakovredna glede na učinek na PEFR in klinično učinkovitost. AF s polovičnim odmerkom je učinkovitejši od ECU pri vplivanju na PEFR. Ti podatki potrjujejo farmakokinetične značilnosti in relativno afiniteto treh preiskovanih zdravil za steroidne receptorje.
Klinična preskušanja, ki primerjajo učinkovitost ICS v obliki izboljšanja simptomov in indikatorjev dihalne funkcije, kažejo, da se UD in BDP v aerosolnih inhalatorjih v enakih odmerkih praktično ne razlikujeta po učinkovitosti, AF zagotavlja enak učinek.vie, kot podvojeni odmerek BDP ali BUD v odmerjenem aerosolu.
Trenutno se aktivno preučuje primerjalna klinična učinkovitost različnih ICS.
INsborov odmerek ICS. Ocenjena priporočena ali optimalna? Kaj je bolj učinkovito?Za zdravnike je zelo zanimiva izbira dnevnega odmerka ICS in trajanja zdravljenja med osnovno terapijo BA za nadzor simptomov astme. Boljšo raven nadzora nad potekom astme hitreje dosežemo z uporabo večjih odmerkov ICS (stopnja dokazov A, tabela 1).
Začetni dnevni odmerek ICS mora biti običajno 400-1000 μg (glede na beklometazon); pri hujših BA lahko priporočamo večje odmerke ICS ali začnemo zdravljenje s sistemskim GCS (C). Standardne odmerke ICS (kar ustreza 800 mcg beklometazona) v primeru neučinkovitosti lahko povečamo na 2000 mcg glede beklometazona (A).
Dokazi o učinkih, povezanih z odmerkom, kot je AF, so različni. Tako nekateri avtorji opažajo od odmerka odvisno povečanje farmakodinamičnih učinkov tega zdravila, drugi raziskovalci pa navajajo, da je uporaba nizkih (100 μg / dan) in visokih odmerkov (1000 μg / dan) AF skoraj enako učinkovita.
Preglednica 1 Rizračunane ekvivalentne doze ICS (μg) A.G. Chuchalin, 2002 v modifikaciji
| Nizko | Povprečno | Visoko | Nizko | Povprečno | Visoko | |
| BDP (Beklozon Eco Light Breathing, Beklat, Beklofort) | 200–500 | 500–1000 | > 1000 | 100- 400 | 400- 800 | > 800 |
| BUD (Budezonid, Budecourt) | 200-400 | 400-800 | > 800 | 100-200 | 200-400 | > 400 |
| GRIPA * | 500-1000 | 1000 2000 | > 2000 | 500 750 | 1000 1250 | > 1250 |
| FP (Flixotide, Flohal) | 100-250 | 250-500 | > 500 | 100-200 | 200-500 | > 500 |
| TA * | 400 -1000 | 1000 2000 | > 2000 | 400 800 | 800 1200 | > 1200 |
* aktivne snovi, katerih pripravki niso registrirani v Ukrajini
Z naraščanjem odmerka pa se ICS povečaresnost njihovih sistemskih neželenih učinkov, medtem ko so v majhnih in srednjih odmerkih ta zdravilapodgane redko povzročajo klinično pomembnereakcije na zdravila in jih zaznamuje dobro razmerje med tveganji in koristmi (raven dokazov A).
Dokazana je visoka učinkovitost ICS, če se daje 2-krat na dan; pri uporabi ICS 4-krat na dan v istem dnevnem odmerku se učinkovitost zdravljenja nekoliko poveča (A).
Pedersen S. et al. je pokazala, da nizki odmerki ICS zmanjšajo pogostnost poslabšanj in potrebo po beta2-adrenergičnih agonistih, izboljšajo parametre FVD, vendar so visoki odmerki teh zdravil potrebni za boljši nadzor vnetnega procesa v dihalnih poteh in največje zmanjšanje bronhialne hiperodzivnosti.
Do nedavnega se ICS ni uporabljal za zdravljenje poslabšanj astme, ker menili, da so pri poslabšanju manj učinkoviti kot sistemski GCS. Številne študije kažejo na visoko učinkovitost jemanja sistemskih kortikosteroidov pri poslabšanjih astme (stopnja dokazov A). Od 90. let prejšnjega stoletja, ko so se pojavili novi aktivni ICS (EUD in AF), pa so jih začeli uporabljati za zdravljenje poslabšanj astme. Številne klinične študije so pokazale, da se učinkovitost ICS BUD in AF v visokih odmerkih v kratkem poteku (2 - 3 tedne) ne razlikuje od učinkovitosti deksametazona pri zdravljenju blagih in hudih poslabšanj astme. Uporaba ICS med poslabšanjem astme omogoča doseganje normalizacije kliničnega stanja bolnikov in kazalnikov dihalne funkcije, ne da bi povzročala stranske sistemske učinke.
V večini študij je bila ugotovljena zmerna učinkovitost ICS pri zdravljenju poslabšanj astme, ki se je gibala med 50 in 70% ob uporabi dvojnega odmerka (od odmerka osnovne terapije) AF, in povečanje učinkovitosti zdravljenja z dodatno uporabo podaljšanega beta 2 - agonista salmeterola za 10–15 %. V skladu s priporočili mednarodnega konsenza o zdravljenju bronhialne astme je alternativa povečanju odmerka zdravila, če z uporabo ICS v majhnih in srednjih odmerkih ni mogoče zagotoviti optimalnega nadzora nad astmo, imenovanje dolgo delujočih β-agonistov.
Izboljšanje učinka ICS v kombinaciji s podaljšanimi agonisti adrenergičnih receptorjev beta2 pri bolnikih s KOPB je bilo dokazano v randomiziranem, dvojno slepem, nadzorovanem preskušanju TRISTAN (preskušanje inhalacijskih steroidov in dolgo delujočih beta2 agonistov), \u200b\u200bki je vključevalo 1465 bolnikov. V primerjavi s kombiniranim zdravljenjem (FP 500 mcg + salmeterol 50 mcg 2-krat na dan) se je pogostnost poslabšanj KOPB zmanjšala za 25% v primerjavi s placebom. Kombinirano zdravljenje je dalo izrazitejši učinek pri bolnikih s hudo KOPB, pri katerih pri katerih je bil začetni FEV1 manjši od 50% vrednostith.
Učinkovitost zdravil, ki se uporabljajo pri AD, je v veliki meri odvisna od načina dostave , kaj vpliva na odlaganje zdravila v dihalih. Pljučno odlaganje zdravil pri uporabi različnih sistemov za dajanje znaša od 4 do 60% danega odmerka. Obstaja jasna povezava med pljučnim nanosom in kliničnim učinkom zdravila. Aerosolni inhalatorji z merjenimi odmerki (MDI), ki so bili uvedeni v klinično prakso leta 1956, so najpogostejše naprave za inhaliranje. Pri uporabi MDI približno 10-30% zdravila (če se vdihne brez distančnika) vstopi v pljuča in nato v sistemski obtok. Večina zdravila, ki je približno 70-80%, se odlaga v ustih in grlu ter pogoltne. Napake pri uporabi MDI dosežejo 60%, vodijo do nezadostne dostave zdravila v dihala in s tem zmanjšajo učinkovitost terapije z ICS. Uporaba distančnika omogoča zmanjšanje porazdelitve zdravila v ustni votlini do 10% in optimizacijo vnosa aktivne snovi v dihala, ker ne zahteva absolutnega usklajevanja pacientovih ukrepov.
Bolj ko je BA hujši pri bolniku, manj učinkovita je terapija z običajnimi dozirnimi aerosoli, saj lahko le 20–40% bolnikov ob njihovi uporabi reproducira pravilno tehniko vdihavanja. V zvezi s tem so v zadnjem času ustvarjeni novi inhalatorji, ki od pacienta ne zahtevajo usklajevanja gibov med vdihavanjem. V teh dostavnih napravah se dostava zdravila aktivira z vdihom bolnika, to je tako imenovani BOI (Breathe Operated Inhaler) - inhalator, ki se aktivira z vdihavanjem. Sem spada inhalator Easi-Breath (lahkotno dihanje z vetrom). Beklazon Eco Light Breathing je trenutno registriran v Ukrajini. Inhalatorji za suhi prah (dipihaler (Flohal, Budekort), diskusi (Flixotide (FP), Seretide - FP + salmeterol), razpršilci - dostavno sredstvo, ki zagotavlja optimalni odmerek ICS in zmanjšuje neželene stranske učinke terapije. , kot dvojni odmerek ECU v odmerjenem aerosolu.
Zgodnje uvedbo protivnetnega zdravljenja z ICS zmanjša tveganje za nepopravljive spremembe v dihalnih poteh in olajša potek astme. Pozno uvedba zdravljenja z ICS posledično privede do nižjih rezultatov funkcionalnih testov (dokaz C).
Randomizirana, dvojno slepa, s placebom nadzorovana študija START (Inhalacijsko zdravljenje s steroidi kot redno zdravljenje v zgodnji študiji astme) je pokazala, da prej kot se začne osnovno zdravljenje za BA ICS, lažje napredovanje bolezni. Rezultati START so bili objavljeni leta 2003. Učinkovitost zgodnjega zdravljenja za EUD je bila potrjena s povečanjem parametrov funkcije dihal.
Dolgotrajno zdravljenje z ICS izboljša ali normalizira delovanje pljuč, zmanjša vsakodnevna nihanja največje hitrosti ekspiratornega pretoka, potrebo po bronhodilatatorjih in GCS za sistemsko uporabo do popolne odpovedi. Poleg tega se s podaljšano uporabo zdravil zmanjša pogostost poslabšanj, hospitalizacij in smrtnosti bolnikov.
Hškodljivi učinki ICS ali varnost zdravljenja
Kljub temu da ima ICS lokalni učinek na dihala, obstajajo nasprotujoče si informacije o pojavu neželenih sistemskih učinkov (NE) ICS, od njihove odsotnosti do izrazitih manifestacij, ki predstavljajo tveganje za bolnike, zlasti za otroke. Ti NE vključujejo zatiranje delovanja nadledvične skorje, učinke na presnovo kosti, podplutbe in redčenje kože, kandidozo ustne votline in nastanek sive mrene.
Prepričljivo je dokazano, da dolgotrajna terapija z ICS ne vodi do pomembnih sprememb v strukturi kostnega tkiva, ne vpliva na metabolizem lipidov, stanje imunskega sistema in ne poveča tveganja za nastanek subkapsularne sive mrene. Vendar se še naprej razpravlja o vprašanjih v zvezi z možnim vplivom ICS na stopnjo linearne rasti otrok in stanje hipotalamično-hipofizno-nadledvičnega sistema (HPA).
Manifestacije sistemskih učinkov so v glavnem odvisne od farmakokinetike zdravila in so odvisne od skupne količine prejetih GCS v sistemsko cirkulacijo (sistemska biološka uporabnost)in vrednost zračnosti GCS. Zato je glavni dejavnik, ki določa učinkovitost in varnost ICS, selektivnost zdravila zav zvezi z dihali - prisotnost visokihnekaj lokalnega protivnetnega delovanja in nizko sistemsko aktivnost (tabela 2).
tabela 2 ... Selektivnost ICS in sistemska aktivnost ICS
| ICS | Lokalna dejavnost | Sistemska aktivnost | Razmerje lokalne / sistemske aktivnosti |
| BUD | 1,0 | 1,0 | 1,0 |
| BJP | 0,4 | 3,5 | 0,1 |
| GRIPA | 0,7 | 12,8 | 0,05 |
| TAA | 0,3 | 5,8 | 0,05 |
Varnost ICS v glavnem določanjegova biološka uporabnost iz prebavil in je obratno sorazmerna z njo. Peperoralna biološka uporabnost različnih ICS se giblje od manj kot 1% do 23%. Vzemimoodstranjevanje distančnika in izpiranje ust po vdihavanju znatno zmanjša peroralno biološko uporabnostrazpoložljivost (raven dokazov B). Peroralna biološka uporabnost je skoraj nič pri AF in 6-13% pri EUD, biološka uporabnost ICS pri vdihavanju pase giblje od 20 (FP) do 39% (FLU).
Sistemska biološka uporabnost ICS je vsota inhalacijske in oralne biološke uporabnosti. Pri BDP je sistemska biološka uporabnost približno 62%, kar je nekoliko višje kot pri drugih ICS.
ICS imajo hiter očistek, njegova vrednost približno sovpada z vrednostjo jetrnega krvnega pretoka in to je eden od razlogov za minimalne manifestacije sistemskega NE. Po prehodu skozi jetra ICS vstopi v sistemsko cirkulacijo predvsem v obliki neaktivnih presnovkov, z izjemo aktivnega presnovka BDP - beklometazon 17-monopropionata (17-BMP) (približno 26%) in le majhen del (od 23% TAA do manj kot 1 % FP) - v obliki nespremenjene droge. Prvi prehod skozi jetra inaktivira približno 99% AF in MF, 90% BUD, 80 90% TAA in 60 70% BDP. Visoka presnovna aktivnost novih ICS (FP in MF, glavna frakcija, ki zagotavlja njihovo sistemsko aktivnost, ni večja od 20% odvzetega odmerka (običajno ne presega 750-1000 μg / dan)) lahko razloži njihov boljši varnostni profil v primerjavi z drugimi ICS. verjetnost razvoja klinično pomembnih neželenih učinkov zdravil je izredno majhna, in če obstajajo, so običajno nepomembni in ne zahtevajo prekinitve zdravljenja.
Vsi našteti sistemski učinki ICS so posledica njihove sposobnosti, da kot agonisti receptorjev GCS vplivajo na hormonsko regulacijo v HPA. Zato je zaskrbljenost zdravnikov in bolnikov, povezanih z uporabo ICS, lahko popolnoma upravičena. Hkrati nekatere študije niso pokazale pomembnega učinka ICS na HPA.
Zanimiv je MF, novi ICS z zelo visoko protivnetno aktivnostjo, ki nima biološke uporabnosti. V Ukrajini ga predstavlja samo pršilo za nos Nazonex.
Nekaterih tipičnih učinkov kortikosteroidov pri uporabi kortikosteroidov še nikoli niso opazili, na primer tistih, ki so povezani z imunosupresivnimi lastnostmi tega razreda zdravil ali z razvojem subkapsularne sive mrene.
Preglednica 3 ODprimerjalne študije ICS, ki so vključevale določitev terapevtskega učinkadotin sistemsko aktivnost osnovnega serumskega kortizola ali ACTH analognega stimulacijskega testa.
| Število bolnikov | ICS / dnevni odmerek μg dveh zdravil | Učinkovitost (jutranji PSV *) | Sistemska aktivnost |
| 672 odraslih | FP / 100, 200, 400, 800 iBDP / 400 | FP 200 \u003d BDP 400 | FP 400 \u003d BDP 400 |
| 36 odraslih | BDP / 1500 in BUD / 1600 | BDP \u003d BUD | BDP \u003d BUD - brez učinka |
| 398 otrok | BDP / 400 in FP / 200 | FP\u003e BDP | FP \u003d BDP - brez učinka |
| 30 odraslih | BDP / 400 in BUD / 400 | BDP \u003d BUD | BDP \u003d BUD - brez učinka |
| 28 odraslih | BDP / 1500 in BUD / 1600 | BDP \u003d BUD | BDP \u003d BUD |
| 154 odraslih | BDP / 2000 in FP / 1000 | FP \u003d BDP | BDP\u003e FP |
| 585 odraslih | BDP / 1000 in FP / 500 | FP \u003d BDP | FP \u003d BDP - brez učinka |
| 274 odraslih | BDP / 1500 in FP / 1500 | FP\u003e BDP | BDP \u003d FP - brez učinka |
| 261 odraslih | BDP / 400 in FP / 200 | FP \u003d BDP | BDP\u003e FP |
| 671 odraslih | BUD / 1600 in FP / 1000,2000 | FP 1000\u003e BUD, FP 2000\u003e BUD | FP 1000 \u003d BUD, FP 2000\u003e BUD |
| 134 odraslih | BDP / 1600 in FP / 2000 | FP \u003d BDP | FP\u003e BDP |
| 518 odraslih | BUD / 1600 in FP / 800 | FP\u003e BUD | BUD\u003e FP |
| 229 otrok | BUD / 400 in FP / 400 | FP\u003e BUD | BUD\u003e FP |
| 291 odraslih | TAA / 800 in FP / 500 | FP\u003e TAA | FP \u003d TAA |
| 440 odraslih | FLU / 1000 in FP / 500 | FP\u003e GRIPA | FP \u003d GRIPA |
| 227 odraslih | BUD / 1200 in FP / 500 | BUD \u003d FP | BUD\u003e FP |
Opomba: * PSV največji pretok izdiha
Odvisnost sistemskega učinka ICS na odmerekzdravilo ni očitno, rezultati študij so si nasprotujoči (tabela 3). Nekljub vprašanjem, ki se nam porajajo, nas predstavljeni klinični primeri dajejo misliti na varnosttveganje za dolgotrajno zdravljenje z visokimi odmerki ICS. Verjetno obstajajo bolniki, ki so zelo občutljivi na zdravljenje s steroidi. Imenovanjevisoki odmerki ICS pri takih osebah lahko povzročijo večjo pojavnost sistemskihstranski učinki. Dejavniki, ki določajo visoko občutljivost pacienta na GCS, še vedno niso znani. Opazimo lahko le, da je število takihje zelo malo bolnikov (4 opisani primeri na16 milijonov bolnikov / let uporabe samoFP od leta 1993).
Najbolj zaskrbljujoča je možnost, da ICS vpliva na rast otrok, saj se ta zdravila običajno uporabljajo dolgo časa. Na rast otrok z astmo, ki ne prejemajo GCS v kakršni koli obliki, lahko vplivajo številni dejavniki, kot so: sočasna atopija, resnost astme, spol in drugi. Otroška astma je verjetno povezana z zaostajanjem v razvoju, čeprav ne povzroči zmanjšanja končne rasti odraslih. Študije so bile namenjene številnim dejavnikom, ki vplivajo na rast pri otrocih z AD ki jih povzroča učinek ICS ali sistemskih kortikosteroidov na rast,imajo nasprotujoče si rezultate.
Lokalni neželeni učinki ICS vključujejo: kandidiazo ustne votline in orofarinksa, disfonijo, včasih kašelj zaradi draženja zgornjih dihal, paradoksalni bronhospazem.
Pri jemanju majhnih odmerkov ICS je pojavnost lokalnih neželenih učinkov majhna. Tako se oralna kandidiaza pojavi pri 5% bolnikov, ki uporabljajo majhne odmerke ICS, in pri do 34% bolnikov, ki uporabljajo visoke odmerke teh zdravil. Disfonijo opazimo pri 5-50% bolnikov, ki uporabljajo ICS; njegov razvoj je povezan tudi z večjimi odmerki zdravil. V nekaterih primerih se pri uporabi ICS lahko razvije refleksni kašelj. Kot odziv na dajanje ICS, izvedeno s pomočjo AIM, se lahko razvije paradoksalni bronhospazem. V klinični praksi jemanje bronhodilatacijskih zdravil pogosto prikrije tovrstno bronhokonstrikcijo.
Tako je ICS bil in ostaja temelj zdravljenja BA pri otrocih in odraslih. Varnost dolgotrajne uporabe majhnih in srednje velikih odmerkov ICS ni dvoma. Dolgotrajno dajanje visokih odmerkov ICS lahko privede do razvoja sistemskih učinkov, najpomembnejši pa so upočasnitev CPR pri otrocih in zatiranje delovanja nadledvične žleze.
Najnovejša mednarodna priporočila za zdravljenje astme pri odraslih in otrocih nakazujejo predpisovanje kombiniranega zdravljenja z ICS in dolgo delujočimi beta-2-agonisti v vseh primerih, kadar uporaba majhnih odmerkov ICS ne daje učinka. Izvedljivost tega pristopa ne potrjuje le njegova večja učinkovitost, temveč tudi boljši varnostni profil.
Predpisovanje visokih odmerkov ICS je priporočljivo le, če je kombinirano zdravljenje neučinkovito. Verjetno bi se moral v tem primeru za uporabo visokih odmerkov ICS odločiti pulmolog ali alergolog. Po doseganju kliničnega učinka je priporočljivo odmerek ICS titrirati na najnižji učinkoviti odmerek. V primeru dolgotrajne terapije z BA z visokimi odmerki ICS je treba izvesti nadzor varnosti, ki lahko vključuje merjenje CPR pri otrocih in določanje ravni kortizola zjutraj.
Ključ do uspešne terapije je odnos bolnika z zdravnikom in odnos bolnika do skladnosti z zdravljenjem.
Ne pozabite, da je to splošna nastavitev. Individualni pristop k zdravljenju bolnikov z BA ni izključen, ko zdravnik izbere zdravilo, režim in odmerek njegovega imenovanja. Če zdravnik na podlagi priporočil sporazumov o obvladovanju astme vodi svoje znanje, obstoječe informacije in osebne izkušnje, potem je uspeh zdravljenja zagotovljen.
LITERATURA
1. Globalna strategija za obvladovanje in preprečevanje astme. Nacionalni inštituti za zdravje, Nacionalni inštitut za srce, pljuča in kri. Revidirano 2005. Publikacija NIH št. 02-3659 // www.ginasthma.co m. Barnes PJ. Učinkovitost inhalacijskih kortikosteroidov pri astmi. J Allergy Clin Immunol 1998; 102 (4 pt 1): 531-8.
2. Barnes N.C., Hallet C., Harris A. Klinične izkušnje s flutikazonpropionatom pri astmi: metaanaliza učinkovitosti in sistemske aktivnosti v primerjavi z budezonidom in beklometazon dipropionatom pri polovici mikrogramskega odmerka ali manj. Respir. Med.1998; 92: 95.104.
3. Pauwels R, Pedersen S, Busse W, et al. Zgodnje posredovanje budezonida pri blagi vztrajni astmi: randomizirano, dvojno slepo preskušanje. Lancet 2003; 361: 1071-76.
4. Glavne določbe poročila strokovne skupine EPR-2: vodilne smernice pri diagnozi in zdravljenju bronhialne astme. Nacionalni inštitut za srce, pljuča in kri. Publikacija NIH N 97-4051A. Maj 1997 / Per. izd. A.N. Choi. M., 1998.
5. Crocker IC, Church MK, Newton S, Townley RG. Glukokortikoidi zavirajo proliferacijo in izločanje interlevkina 4 in interlevkina 5 s pomočjo celičnih linij tipa 2 tipa 2 za aeroalergene. Ann Allergy Asthma Immunol 1998; 80: 509-16.
6. Umland SP, Nahrebne DK, Razac S, et al. Inhibitorni učinek lokalno aktivnih glukokortikoidov na tvorbo IL4, IL5 in interferona gama s pomočjo gojenih primarnih CD4 + T celic J. Allergy Clin. Immunol 1997; 100: 511-19.
7. Derendorf H. Farmakokinetik in farmakodinamične lastnosti inhalacijskih kortikosteroidov pri učinkovitosti in varnosti. Respir med1997; 91 (dodatek A): 22-28.
8. Johnson M. Farmakodinamika in farmakokinetiki inhalacijskih glukokortikoidov. J Allergy Clin Immunol 1996; 97: 169-76.
9. Brokbank W, Brebner H, Pengelly CDR. Kronična astma, zdravljena z aerosolnim hidrokortizonom. Lancet 1956: 807.
10. Raziskovalna skupina za program upravljanja otroške astme. Dolgoročni učinki budezonida ali nedokromila pri otrocih z astmo // N. Engl. J.Med. - 2000. - Letn. 343. - str. 1054-1063.
11. Suissa S, Ernst P. // J Allergy Clin Immunol.-2001.-letnik 107, št. 6.-P.937-944.
12. Suissa S., Ernst P., Benayoun S. et al. // N Engl J Med.-2000.-letnik 343, št. 5.-P.332. Lipworth B.J., Jackson C.M. Varnost inhalacijskih in intranazalnih kortikosteroidov: lekcije za novo tisočletje // Drug Safety. - 2000. - Letn. 23. - str. 11–33.
13. Smolenov I.V. Varnost inhalacijskih glukokortikosteroidov: novi odgovori na stara vprašanja // Atmosfera. Pulmologija in alergologija. 2002. št. 3. - C. 10-14.
14. Burge P, Calverley P, Jones P, et al. Randomizirana, dvojno izmerjena, s placebom nadzorovana študija flutikazonpropionata pri bolnikih z zmerno do hudo kronično obstruktivno pljučno boleznijo: preskušanje ISOLDE. BMJ 2000; 320: 1297-303.
15. Sutochnikova O. A., Chernyaev A. L., Chuchalin A. G. Inhalacijski glukokortikosteroidi pri zdravljenju bronhialne astme // Pulmologija. –1995. - Zvezek 5. - str. 78 - 83.
16. Allen D. B., Mullen M., Mullen B. Metaanaliza učinka peroralnih in inhalacijskih kortikosteroidov na rast // J. Allergy Clin. Imunol. - 1994. - Letn. 93. - str. 967-976.
17. Hogger P, Ravert J, Rohdewald P. Raztapljanje, vezava na tkivo in kinetiki vezave receptorjev za inhalirane glukokortikoide. Eur Respir J 1993; 6 (dodatek 17): 584S.
18. Tsoi A.N. Farmakokinetični parametri sodobnih inhalacijskih glikokortiko-steroidov // Pulmologija. 1999. Št. 2. S. 73-79.
19. Miller-Larsson A., Maltson R. H., Hjertberg E. et al.Reverzibilna konjugacija maščobnih kislin budezonida: nov mehanizem za dolgotrajno zadrževanje lokalno uporabljenega steroida v tkivu dihalnih poti // Drug.metabol. Odstranitve. 1998; v. 26 N 7: 623-630.A. K., Sjodin, Hallstrom G. Reverzibilno tvorjenje estrov maščobe kisline budezonida, glukokortikoida proti astmi, v človeških mikrosomih pljuč in jeter // Zdravilo. Presnovni. Odstranitve. 1997; 25: 1311-1317.
20. Van den Bosch J. M., Westermann C. J. J., Edsbacker J. et al. Povezava med koncentracijami inhaliranega budezonida v pljučnem tkivu in krvni plazmi // Biopharm Drug. Odstranitve. 1993; 14: 455-459.
21. Wieslander E., Delander E. L., Jarkelid L. et al.Farmakološki pomen reverzibilne konjugacije maščobe kisline budezonida, nastale v celični liniji podgan in vitro // Am. J. Respir. Celica. Mol. Biol. 1998; 19: 1–9.
22. Thorsson L., Edsbacker S. Conradson T. B. Odlaganje budezonida iz pljuč Turbuhalerja v pljučih je dvakrat večje kot pri inhalatorju p-MDI pod tlačnim odmerkom // Eur. Respir. J. 1994; 10: 1839-1844
23. Derendorf H. Farmakokinetične in farmakodinamične lastnosti inhalacijskih kortikosteroidov glede na učinkovitost in varnost // Respir. Med. 1997; 91 (Priloga A): 22-28
24. Jackson W. F. Nebulizirana terapija z budezonidom v znanstvenem in praktičnem pregledu astme. Oxford, 1995: 1-64
25. Trescoli-Serrano C., Ward W. J., Garcia-Zarco M. et al. Gastrointestina absorpcije inhaliranega budezonida in beklometazona: ali ima kakšen pomemben sistemski učinek? // Am. J. Respir. Kritično. Care Med. 1995; 151 (št. 4 del 2): \u200b\u200bA. Borgstrom L. E, Derom E., Stahl E. et al. Inhalacijska naprava vpliva na odlaganje pljuč in bronhodilatacijski učinek terbutalina // Am. J. Respir. Kritično. Care Med. 1996; 153: 1636-1640.
26. Ayres J.G., Bateman E.D., Lundback E., Harris T.A.J. Visoki odmerki flutikazonpropionata, 1 mg na dan, v primerjavi s flutikazon propionatom, 2 mg na dan, ali budezonida, 1,6 mg na dan, pri bolnikih s kronično hudo astmo // Eur. Respir. J. - 1995. - letnik 8 (4). - str. 579-586.
27. Boe J., Bakke P., Rodolen T., et al. Visokoodmerni inhalacijski steroidi pri astmatikih: zmerno povečanje učinkovitosti in zatiranje osi hipotalamus hipofiza-nadledvična žleza (HPA) // Eur. Respir. J. –1994. - Zv. 7. - str. 2179-2184.
28. Dahl R., Lundback E., Malo J. L., et al. Študija določanja odmerka flutikazonpropionata pri odraslih bolnikih z zmerno astmo // Prsni koš. - 1993. - Letn. 104. - str. 1352-1358.
29. Daley-Yates P.T., Price A.C., Sisson J.R. et al.Beklometazon dipropionat: absolutna biološka uporabnost, farmakokinetika in metabolizem po intravenski, peroralni, intranazalni in inhalacijski uporabi pri človeku // J. Clin. Pharmacol. - 2001. - Letn. 51. - str. 400-409.
30. Mollmann H., Wagner M., Meibohm B. et al.Farmakokinetični in farmakodinamični razvoj flutikazonpropionata po inhalacijiticija // Eur. J. Clin. Pharmacol. - 1999. - Letn. 53.-P. 459-467.
31. Ninan T. K., Russell G. Astma, zdravljenje z inhalacijskimi kortikosteroidi in rast, Arch. Dis. Otrok. –1992. - Zv. 67 (6). - str. 703 705.
32. Pedersen S., Byrne P. O. Primerjava učinkovitosti in varnosti inhalacijskih kortikosteroidov pri astmi // Eur. J. Alergija. Clin. Imunol. - 1997. - V.52 (39). - P.1-34
33. Thompson P. I. Dostava drog v majhne dihalne poti // Amer. J. Repir. Kritično. Med. - 1998. - V. 157. - P.199 - 202.
34. Boker J., McTavish D., budezonid. Posodobljen pregled njegovih farmakoloških lastnosti in terapevtske učinkovitosti pri astmi in rinitisu // Zdravila. –1992. - v. 44. - št. 3. - 375 - 407.
35. Calverley P, Pauwels R, Vestibo J, et al. Kombinirani salmeterol in flutikazon pri zdravljenju kronične obstruktivne pljučne bolezni: randomizirano nadzorovano preskušanje. Lancet 2003; 361: 449-56.
36. Ocena vnetja dihalnih poti pri astmi / A.M. Vignola. J. Bousquet, P. Chanez et al. // Am. J. Respir. Kritično. Care Med. - 1998. - V. 157. - str. 184-187.
37. Yashina L.O., Gogunska I.V. Učinkovitost in varnost inhalacijskih kortikosteroidov pri zdravljenju vnetja bronhialne astme // Astma in alergija. - 2002. št. 2. - str. 21 - 26.
38. Učinkovitost in varnost inhalacijskih kortikosteroidov pri nadzoru akutnih napadov astme pri otrocih, ki so bili zdravljeni na oddelku za nujne primere: nadzorovana primerjalna študija s peroralnim prednizolonom / B. Volovits, B. Bentur, Y. Finkelshtein et al. // J. Allergy Clin. Imunol. - 1998. - V. 102. - N. 4. - str. 605 - 609.
39. Sinopalnikov A.I., Klyachkina I.L. Sredstva za dovajanje zdravil v dihala pri bronhialni astmi // Ruske medicinske novice. -2003. Št. 1. S. 15-21.
40. Nicklas RA. Paradoksalni bronhospazem, povezan z uporabo inhalacijskih beta agonistov. J Allergy Clin Immunol 1990; 85: 959-64.
41. Pedersen S. Astma: Osnovni mehanizmi in klinično vodenje. Ed. P. J. Barnes. London 1992, str. 701-722
42. Ebden P., Jenkins A., Houston G., et al. Primerjava dveh velikih odmerkov kortikosteroidnega aerosola, beklometazondipropionata (1500 mcg / dan) in budezonida (1600 mcg / dan), za kronično astmo // Thorax. - 1986. - Letn. 41. - P.869-874.
43. Brown P. H., Matusiewicz S. P., Shearing C. et al. Sistemski učinki visokih odmerkov vdihanih steroidov: primerjava beklometazon dipropionata in budezonida pri zdravih osebah // Thorax. - 1993.– letn. 48. - str. 967-973.
44. Varnost inhalacijskih in intranazalnih kortikosteroidov: lekcije za novo tisočletje // Varnost drog. –2000. - Zv. 23. - str. 11–33.
45. Doull I.J.M., Freezer N.J., Holgate S.T. Rast predpubertetnih otrok z blago astmo, zdravljenih z inhalacijskim beklometazon dipropionatom // Am. J.Respir. Kritično. Care Med. - 1995. - Letn. 151. - str. 1715-1719.
46. \u200b\u200bGoldstein D.E., Konig P. Vpliv inhalacijskega beklometazon dipropionata na delovanje osi hipotalamp hipofiza-nadledvična žleza pri otrocih z astmo // Pediatrija. - 1983. - Letn. 72. - str. 60-64.
47. Kamada A.K., Szefler S.J. Glukokortikoidi in rast pri astmatičnih otrocih // Pediatr. Alergija Immunol. - 1995. - Letn. 6. - str. 145-154.
48. Prahl P., Jensen T., Bjerregaard-Andersen H. Adrenokortikalna funkcija pri otrocih na visokih odmerkih steroidnih aerosolnih terapij // Alergija. - 1987. - letnik 42. - str. 541-544.
49. Priftis K., Milner A.D., Conway E., Honor J. W. Nadledvična funkcija pri astmi // Arch. Dis. Otrok. –1990. - Zv. 65. - str. 838-840.
50. Balfour-Lynn L. Rast in otroška astma // Arch. Dis. Otrok. - 1986. - Letn. 61 (11). - str. 1049-1055.
51. Kannisto S., Korppi M., Remes K., Voutilainen R. Supresija nadledvične žleze, ovrednotena z nizkoodmernim testom adrenokortikotropina in rast pri astmatičnih otrocih, zdravljenih z vdihanimi steroidi // Journal of Clinical Endocrinology and Metabolism. - 2000. - Letn. 85. - str. 652 - 657.
52. Prahl P. Adrenokortikalna supresija po zdravljenju z beklometazon dipropionatom in budezonidom // Clin. Exp. Alergija. - 1991. - Letn. 21.– str. 145-146.
53. Tabachnik E., Zadik Z. Dnevno izločanje kortizola med terapijo z inhalacijskim beklometazon dipropionatom pri otrocih z astmo // J. Pediatr. –1991. - Zv. 118. - str. 294-297.
54. Capewell S., Reynolds S., Shuttleworth D. et al.Purpura in redčenje kože, povezano z vdihavanjem velikih odmerkov kortikosteroidov // BMJ. - 1990. letnik 300. - str. 1548-1551.
Prvi topični inhalacijski glukokortikosteroid je bil ustvarjen le 30 let po odkritju samih glukokortikosteroidov. To zdravilo je bil dobro znani beklometazon dipropionat. Leta 1971 se je uspešno uporabljal za zdravljenje alergijskega rinitisa, leta 1972 pa za zdravljenje bronhialne astme. Kasneje so nastali še drugi hormoni za vdihavanje. Trenutno so topični glukokortikosteroidi zaradi izrazitega protivnetnega antialergijskega učinka in nizke sistemske aktivnosti postali prva zdravila v osnovni terapiji bronhialne astme - glavno zdravljenje, namenjeno doseganju nadzora nad boleznijo.
Od sistemskih se ne razlikujejo le po načinu dajanja, temveč tudi po številnih lastnostih: lipofilnost, nizek odstotek absorpcije v kri, hitrost inaktivacije in kratek razpolovni čas iz krvne plazme. Njihova visoka učinkovitost jim omogoča uporabo v zelo majhnih odmerkih, merjenih v mikrogramih, le majhen del inhalacijskega odmerka pa se absorbira v kri in ima sistemski učinek. V tem primeru se zdravilo hitro inaktivira, kar še dodatno zmanjša možnost sistemskih zapletov. Zaradi teh lastnosti sta pogostnost in resnost neželenih učinkov tudi pri dolgotrajnem zdravljenju z lokalnimi glukokortikosteroidi večkrat nižja kot pri sistemskih hormonih.
Kljub temu številni bolniki in celo nekateri zdravniki strahove, ki jih je povzročila sistemska hormonska terapija, prenašajo na inhalacijske hormone, pa tudi mešajo koncepte "dolgotrajne vzdrževalne terapije za nadzor bolezni" in "odvisnosti od drog". Včasih to privede do nerazumne zavrnitve potrebnega zdravljenja ali do poznega začetka ustreznega zdravljenja, kar lahko privede do nenadzorovanega poteka bronhialne astme in razvoja življenjsko nevarnih zapletov, njihovo zdravljenje pa bo zahtevalo uporabo sistemskih hormonov, katerih stranski učinki samo vzbujajo upravičeno zaskrbljenost. Poleg tega so študije pokazale, da prej kot se začne zdravljenje bronhialne astme, učinkovitejše je, manj terapije bo potrebno za nadzor bolezni.
Dolgotrajen nenadzorovan potek astme vodi tudi v razvoj sklerotičnih procesov v bronhialnem drevesu, kar lahko povzroči pritrditev ireverzibilne bronhialne obstrukcije. Da bi se temu izognili, je nujna tudi zgodnja terapija z inhalacijskimi hormoni, ki ne samo zmanjšajo aktivnost vnetja v bronhialnem drevesu, temveč tudi zavirajo razmnoževanje in aktivnost fibroblastov ter preprečujejo razvoj sklerotičnih procesov.
Inhalirani glukokortikosteroidi za zdravljenje bronhialne astme z njihovo dolgotrajno uporabo normalizirajo pljučno funkcijo, zmanjšajo nihanja največje hitrosti ekspiratornega pretoka, preprečijo zmanjšano občutljivost na beta-2-agoniste, izboljšajo kakovost življenja, zmanjšajo pogostnost poslabšanj in hospitalizacij ter preprečijo razvoj ireverzibilne bronhialne obstrukcije. Zaradi tega veljajo za zdravila prve izbire pri zdravljenju trajne bronhialne astme katere koli resnosti, začenši z blago.
© Nadezhda Knyazheskaya
Novi članki
- Prevzem nadzora nad problematičnim območjem!
- Pet nasvetov za spremembo glasu
- Kaj pričakovati od naslednje epizode
- Hacked Just Dance Now
- Kaj in kako narediti nož v naravi
- Tam, kjer se luna zdi največja
- Vojna se začne v vesolju: vesoljska komunikacija
- Zasebni strežnik Clash of Clans
- Hacked Clash of Clans
- Nosečnost iz dneva v teden, iz tedna v teden
Priljubljeni članki
- Kam napisati ime nove rakete
- So inovativne tehnologije koristne v gradbeništvu?
- Olje iz skrilavca - kaj je to?
- Vojaška vozila in mehanizmi Catapult leonardo da vinci
- Gran Turismo (serija video iger)
- Kako je videti perspektivni moški?
- Ruske žene libanonskih mož: kaj jih pripelje na Bližnji vzhod
- Ženska angleška imena
- Pomanjkanje moških na Islandiji
- Pomen besede žigolo. Gigalo - kdo je to? Določite pomen besede. Žigolo je boljši kot ljubimec za eno noč
